|
|
|
|
|
Глава 4. Изменение агрегатных состояний вещества, газов и твёрдых тел § 27. Плавление и отвердевание кристаллических веществВ каких агрегатных состояниях может находиться вещество? Каково строение кристаллических тел и жидкостей? 1. Рассмотрим процесс превращения вещества из твёрдого состояния в жидкое. Для этого проделаем опыт. Во внутренний сосуд калориметра положим немного измельчённого льда при температуре -10 °С, опустим в него термометр и оставим на столе. Будем следить за изменением температуры льда и процессами, которые с ним происходят. Наблюдения показывают, что какое-то время лёд остаётся в твёрдом состоянии и его температура постепенно повышается. При температуре 0 °С лёд начинает плавиться, в сосуде появляется вода, а температура льда остаётся неизменной до тех пор, пока он весь не перейдёт в жидкое состояние. После этого температура образовавшейся изо льда воды начинает повышаться, и это будет происходить до тех пор, пока она не станет равной комнатной. Таким образом, мы наблюдали переход льда из твёрдого состояния в жидкое.
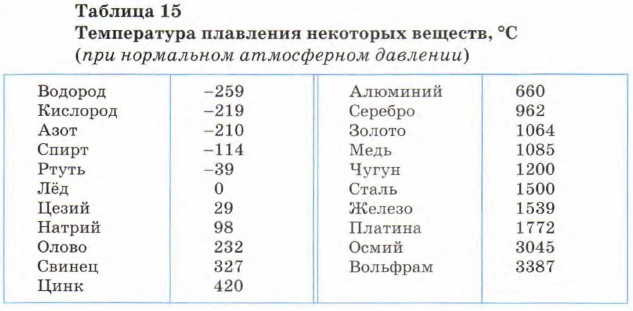
Из наблюдений следует, во-первых, что лёд начинает плавиться при определённой температуре. Важно отметить, что лёд находится в кристаллическом состоянии. Следовательно, процесс плавления кристаллических тел происходит при определённой температуре, которую называют температурой плавления. Во-вторых: температура льда и образовавшейся воды во время всего процесса плавления остаётся неизменной. Таким образом, во время процесса плавления кристаллического вещества температура вещества остаётся постоянной. 2. Лёд участвовал в теплообмене с окружающим воздухом и сосудом калориметра. Получая от них некоторое количество теплоты, лёд нагревался до температуры 0 °С, его внутренняя энергия увеличивалась за счёт увеличения средней кинетической энергии теплового движения его молекул. Затем лёд плавился, и температура его при этом не менялась, но лёд получал некоторое количество теплоты. Следовательно, его внутренняя энергия увеличивалась, но не за счёт кинетической, а за счёт потенциальной энергии взаимодействия молекул. Получаемая извне энергия расходовалась на разрушение кристаллической решётки. Процесс плавления кристаллических тел протекает аналогично рассмотренному процессу плавления льда. Чтобы расплавить твёрдое кристаллическое тело, необходимо нагреть его до температуры плавления и в дальнейшем сообщать ему энергию до тех пор, пока всё оно не превратится в жидкость. Исключение составляют те вещества, которые меняют свой химический состав или сразу превращаются в газ. Различные кристаллические вещества имеют разную температуру плавления (табл. 15).
3. Если вынести сосуд с водой на улицу в зимнее время, через некоторое время вода превратится в лёд.
В рассматриваемом примере вода сначала будет охлаждаться до О °С, отдавая при этом некоторое количество теплоты окружающему воздуху. При этом будет уменьшаться её внутренняя энергия за счёт уменьшения средней кинетической энергии движения молекул. Когда температура воды станет равной О °С, она начнёт превращаться в лёд. При этом температура воды не будет изменяться до тех пор, пока вся она не перейдёт в твёрдое состояние. Этот процесс сопровождается выделением определённого количества теплоты и соответственно уменьшением внутренней энергии воды за счёт уменьшения потенциальной энергии взаимодействия её молекул. Таким образом, переход вещества из жидкого состояния в твёрдое кристаллическое происходит при определённой температуре, называемой температурой кристаллизации. Эта температура остаётся неизменной во время всего процесса кристаллизации. Опыт показывает, что для кристаллических тел температура кристаллизации равна температуре плавления.
|
|
|