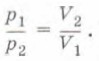|
|
|
|
|
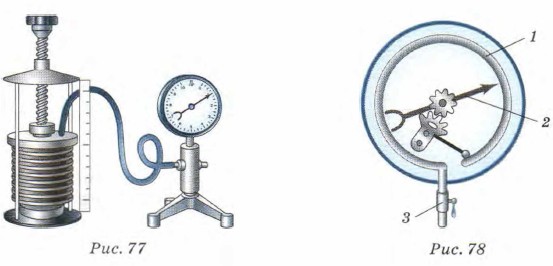
Глава 5. Тепловые свойства газов, жидкостей и твёрдых тел, газов и твёрдых тел § 31. Связь между параметрами состояния газаЧто называют параметрами состояния газа? Каково строение газов? 1. Рассмотрим такие изменения состояния газа, при которых один из параметров, характеризующих его состояние, остаётся постоянным. Пусть изменяются давление и объём некоторого газа, например воздуха, а масса и температура при этом остаются постоянными. Возникает вопрос, как при изменении объёма газа будет изменяться его давление. Для ответа на этот вопрос вспомним, что происходит, если сжимать руками воздушный шарик. При сжатии его объём уменьшается, а давление воздуха в нём увеличивается. Подобные наблюдения позволяют сделать предположение о том, что при увеличении объёма газа его давление уменьшается; при уменьшении объёма давление возрастает. Чтобы проверить это предположение и установить количественную зависимость между давлением и объёмом газа, проделаем опыт. Возьмём цилиндр переменного объёма и соединим его с металлическим манометром (рис. 77). Основной частью манометра является согнутая в форме дуги металлическая трубка 1 (рис. 78). Один её конец закрыт. К её закрытому концу присоединена стрелка 2, которая может перемещаться по шкале прибора. Другой конец трубки 3 соединяют с сосудом, в котором измеряют давление. При увеличении давления в сосуде трубка разгибается и движение её запаянного конца передаётся стрелке.
Будем медленно сжимать воздух в цилиндре, вращая прикреплённый к нему стержень с винтовой нарезкой. Медленное сжатие позволяет сохранить неизменной температуру воздуха, поскольку в этом случае успевает происходить теплообмен между воздухом в цилиндре, стенками цилиндра и окружающим воздухом. 2. Измерения показывают, что произведение давления газа данной массы и его объёма при постоянной температуре одинаково для всех состояний газа: pV = const. Если р1 — давление газа в первом состоянии, V1 — объём газа в первом состоянии, а р2 и V2 — соответственно давление и объём газа во втором состоянии, то можно записать:
Это равенство можно переписать иначе: Таким образом,
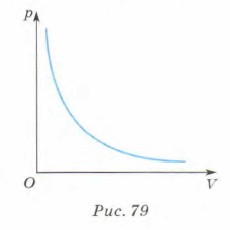
Графиком зависимости давления газа данной массы от его объёма при постоянной температуре является гипербола (рис. 79).
3. Объясним полученную зависимость, используя знания о строении газов. Как вам известно, давление газа обусловлено ударами его молекул о стенки сосуда. При уменьшении объёма газа увеличивается его плотность, т. е. увеличивается число молекул в единице объёма. Соответственно большее число молекул ударяется о стенки сосуда и давление газа возрастает. Возникает вопрос, для всех ли газов справедлива полученная зависимость. Многочисленные опыты показывают, что не для всех и не всегда. Она несправедлива для газов, имеющих большую плотность, а также для газов, находящихся при низких температурах и высоких давлениях. Так, полученная зависимость давления газа от его объёма при постоянной температуре достаточно точно выполняется для водорода, имеющего наименьшую плотность (0,09 кг/м3 при 0 °С в достаточно большом температурном 0 °С) интервале. Для воздуха отклонения от этой зависимости заметны при температуре ниже 0 °С и давлении выше 106 Па.
|
|
|