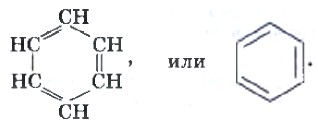|
|
|
|
|
Глава 1. Углеводороды и их природные источники § 7. Арены. БензолБензол С6Н6 является первым представителем аренов. Его можно получить тримеризацией ацетилена:
В больших количествах бензол получают переработкой каменного угля. Ф. Кекуле предложил следующую структурную формулу бензола:
Несмотря на высокую степень непредельности молекулы бензола (по составу), он не дает характерных для алкенов и алкинов качественных реакций: не обесцвечивает бромную воду и раствор перманганата калия. Это связано с особым строением молекулы бензола, которое в настоящее время показывают следующей структурной формулой:
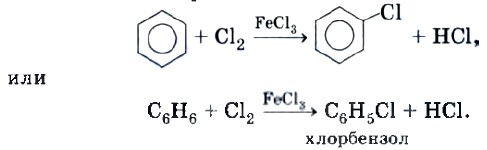
и подробно изучают в курсе органической химии для школ и классов естественнонаучного профиля. Для вас достаточно иметь общее представление о строении молекулы бензола, которое представлено на рисунке 25. Бензол — это бесцветная жидкость с резким характерным запахом, легче воды и нерастворима в ней. Бензол токсичен, поэтому работа с ним в условиях школы недопустима. Рассмотрим химические свойства бензола. Как и все углеводороды, бензол горит: 2С6Н6 + 15O2 → 12СO2 + 6Н2O. Пламя бензола коптящее из-за высокого содержания углерода в молекуле. Бензол используют как добавку к моторному топливу, так как он повышает качество бензина. Однако количество добавляемого бензола строго регламентировано из-за его токсичности. В силу особенностей строения молекулы бензол занимает как бы промежуточное положение между предельными углеводородами (алканами) и непредельными (алкенами), т. е. может вступать как в реакции замещения, так и в реакции присоединения. Однако, в отличие от алканов, реакции замещения с бензолом протекают легче, а реакции присоединения — труднее, чем у алкенов. Последние мы рассматривать не будем, остановимся лишь на реакциях замещения, так как в результате этих реакций образуются вещества, которые используют для производства практически важных продуктов. Реакция хлорирования бензола протекает в присутствии катализатора:
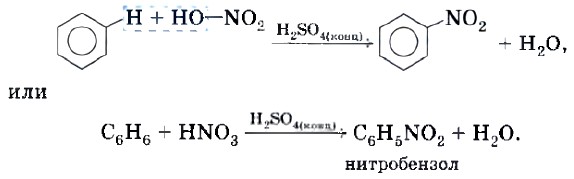
Полученный продукт называют также фенилхлоридом, так как одновалентный радикал С6Н5— называют фенилом. Реакция нитрования — это взаимодействие бензола с азотной кислотой HNO3. Эта реакция протекает в присутствии концентрированной серной кислоты в качестве катализатора:
Полученный продукт называют нитробензолом. Почему нитробензолом? Потому что группу атомов —NO2 называют нитрогруппой. Нитробензол — исходное вещество для получения анилина, который будет рассмотрен в § 16. Области применения бензола показаны на рисунке 26.
1. Как вы думаете, при горении какого углеводорода — бензола или ацетилена — пламя будет более коптящим? Почему? Ответ подтвердите расчетами. 2. Перечислите области применения бензола. 3. Рассчитайте количество вещества ацетилена, который потребуется для получения 400 мл бензола (плотность 0,8 г/мл). 4. Запишите уравнения реакций, с помощью которых можно 4 осуществить следующие превращения: а) метан----> ацетилен----> бензол----> хлорбензол; б) карбонат кальция----> оксид кальция----> карбид кальция ----> ацетилен----> бензол----> нитробензол. 5. Бензол является прекрасным растворителем органических ° веществ и входит в состав многих бытовых препаратов-растворителей, например в состав «Сольвента», где его содержание составляет 25%. Рассчитайте массу бензола, которая необходима для изготовления 300 г «Сольвента».
|
|
|