|
|
|
|
|
Глава 1. Введение в органическую химию Отличительные признаки органических соединенийПроблема. Как экспериментально отличить органическое вещество от неорганического?
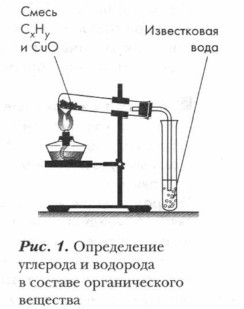
Пробирка с исходными веществами должна быть закреплена в штативе под прямым углом или с небольшим наклоном вниз. Пробирку со смесью осторожно нагревайте в пламени горелки, опустите затем газоотводную трубку в другую пробирку, на 1/4 заполненную известковой водой — насыщенным раствором гидроксида кальция Са(ОН)2 (рис. 1). Что наблюдаете? Какую роль в данном эксперименте играют оксид меди и гидроксид кальция? Какие элементы, входящие в состав органического вещества, вы обнаружили с помощью этого опыта? Когда вы обнаружите слой восстановленной меди, подняв лапку штатива, выньте газоотводную трубку из пробирки с известковой водой, нагревание прекратите. По помутнению известковой воды вы могли определить, что при накаливании органического вещества выделился углекислый газ, следовательно, в составе органического вещества был углерод. По капелькам воды, которая сконденсировалась на стенках нагреваемой пробирки, можно сделать вывод о наличии в составе испытуемого вещества водорода. Это превращение органического соединения можно выразить следующей схемой:
На основе результатов качественного и количественного анализа вещества можно установить его молекулярную формулу. Приведем пример решения подобной задачи. Задача. При сжигании газообразного углеводорода с плотностью по водороду 21 получено 8,4 л оксида углерода (IV) (н. у.) и 6,75 г воды. Определите молекулярную формулу углеводорода.
Если в дополнение к качественному эксперименту осуществить количественный эксперимент, т. е. уловить полученные продукты и определить их массу или объем, то на основе этих данных можно вычислить соотношения атомов в молекуле и составить эмпирическую формулу С выводом химической формулы воды на основе эксперимента по ее синтезу в эвдиометре вы уже знакомились в курсе химии 8 класса. И наоборот, по формуле вещества, установленной на основании количественных экспериментальных данных, можно вычислить относительную молекулярную массу вещества (см. задачу). Молекулы органических веществ образованы достаточно прочными ковалентными связями, следовательно, эти вещества весьма устойчивы. Одной из причин многообразия органических соединений является способность атомов углерода химически связываться друг с другом, образуя углеродные цепи (углеродный скелет) разной длины и структуры. В зависимости от структуры углеродного скелета органические вещества делятся на циклические и ациклические. Напомним, что циклические углеводороды имеют углеродную цепь, замкнутую в цикл, а ациклические соответственно — незамкнутую. Примерами первых могут служить бензол, циклогексан и др., вторых — алканы.
|
|
|



 Лабораторный опыт. Смешайте выданное вам органическое вещество (например, парафин, вазелин и др.) с порошком оксида меди (II) и поместите смесь в сухую пробирку. Пробирку закройте пробкой с газоотводной трубкой, согнутой под прямым углом.
Лабораторный опыт. Смешайте выданное вам органическое вещество (например, парафин, вазелин и др.) с порошком оксида меди (II) и поместите смесь в сухую пробирку. Пробирку закройте пробкой с газоотводной трубкой, согнутой под прямым углом.
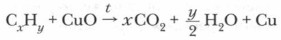
 Если вещество состоит не только из элементов углерода и водорода, остальные его составные части минерализуются, т. е. переходят в неорганические соединения. Содержащиеся в нем такие элементы, как галогены, сера, фосфор и др., обычно обнаруживаются с помощью качественных реакций на соответствующие им ионы.
Если вещество состоит не только из элементов углерода и водорода, остальные его составные части минерализуются, т. е. переходят в неорганические соединения. Содержащиеся в нем такие элементы, как галогены, сера, фосфор и др., обычно обнаруживаются с помощью качественных реакций на соответствующие им ионы.
