|
|
|
|
|
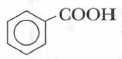
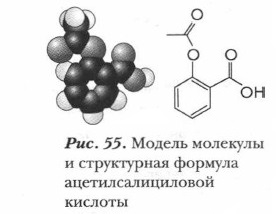
Дополнительный материал к § 31-33 Краткие сведения о некоторых двухосновных, ароматических и прочих карбоновых кислотах (окончание)Образуется в результате деятельности молочнокислых бактерий: свежее молоко быстро населяется этими бактериями, расщепляющими особый молочный сахар — лактозу. Бактерии, получая необходимую для их жизнедеятельности энергию, выделяют молочную кислоту (см. § 41), а молоко под влиянием накапливающейся кислоты свертывается. Молочная кислота придает острый вкус не только скисшему молоку, но и другим продуктам: соленым огурцам, квашеной капусте и т. п. В организме человека молочная кислота образуется при расщеплении глюкозы и служит самостоятельным источником энергии. Например, сердце (как и некоторые иные органы) получает энергию, необходимую для жизнедеятельности, за счет окисления молочной кислоты. К двухосновным оксикарбоновым кислотам относятся яблочная (содержится в яблоках, виноградном соке, недозрелой рябине, клюкве, малине), винная, мезовинная кислоты. Типичной трехосновной оксикарбоновой кислотой является лимонная (рис. 54). Она содержится в смородине, крыжовнике, свекольном соке, недозрелых лимонах. В промышленности ее получают в процессе лимонно-кислого брожения и применяют в кондитерском производстве. Приведем пример, иллюстрирующий роль карбоновых кислот в метаболизме растений. Неспелые плоды жесткие и кисло-горькие на вкус. Этот вкус обусловлен присутствием большого количества органических кислот. По мере созревания плода концентрация кислот понижается: они расходуются в процессе жизнедеятельности. В результате окисления высвобождается энергия, обеспечивающая рост клеток. Созревая, фрукты становятся слаще, что объясняется разрушением молекул крахмала и накоплением образующихся при этом молекул сладкой глюкозы. Не менее обширным является класс ароматических карбоновых кислот, из числа которых вы знакомы с бензойной: Данную область органических соединений также представляют одно- и многоосновные кислоты, в том числе ароматические соединения, содержащие одну или несколько карбоксильных групп. В качестве примера рассмотрим ацетилсалициловую кислоту (рис. 55).
Это всем известный лекарственный препарат аспирин. Он синтезирован в 1899 г. и широко используется при головных болях, а также в качестве жаропонижающего средства. Есть у аспирина и иные области применения. Например, вместе с лимонной кислотой и питьевой содой он входит в состав сельтерской воды. Когда смесь этих веществ добавляют к воде, аспирин превращается в более растворимую натриевую соль и вместе с лимонной кислотой разлагает гидрокарбонат натрия (питьевую соду) до оксида углерода. В результате получается шипучий напиток с приятным вкусом.
|
|
|