|
|
|
|
|
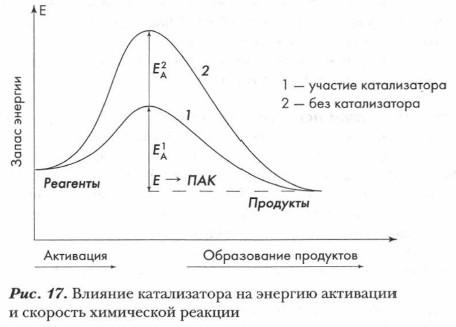
Глава 4. Теоретические основы, механизмы и закономерности протекания реакций органических соединений § 7. Теоретические основы протекания органических реакций (окончание)Катализаторами называются вещества, которые изменяют скорость реакции, участвуют в ней как реагенты, образуя промежуточные активные комплексы (ПАК), но не входят в состав конечных продуктов реакции. Вещества, снижающие скорость реакции, называют ингибиторами. Это приводит к существенному снижению величины энергии активации и, соответственно, к увеличению скорости химической реакции (рис. 1 7).
Природа каталитических органических реакций зависит от типа катализа. Наряду с известными уже вам катализаторами в органической химии, особенно в реакциях, протекающих в живых организмах, распространен и исключительно важен ферментативный катализ, который осуществляется при помощи ферментов (энзимов) — специфичных биокатализаторов белковой природы.
В органических реакциях имеют место следующие виды катализа. 1. Гомогенный катализ осуществляется преимущественно в газовой и жидкой среде, где катализатор и реагенты находятся в одной фазе. Функции катализаторов здесь чаще всего выполняют кислоты и основания. Примером гомогенного катализа может служить каталитическое окисление этилена до уксусного альдегида, промышленное получение уксусной кислоты из углеводородов нефти, например прямым окислением бутана. 2. Гетерогенный катализ протекает при реакциях на поверхности раздела фаз, где катализатор находится в другой фазе (как правило, твердой) по сравнению с реагентами. Примером такого типа катализа могут служить реакции промышленных способов получения аренов из ароматических соединений, получения анилина из нитробензола, которые идут в присутствии катализаторов — металлов, их оксидов и других соединений металлов. Конкретным примером может служить промышленное получение метилового спирта из смеси оксида углерода и водорода (синтез-газ) в присутствии катализаторов — оксидов цинка и хрома и др. (подробнее об этом вы узнаете позже). Следует отметить специфичность действия катализаторов. Универсальных катализаторов для изменения скорости любой реакции нет. 3. Ферментативный катализ имеет место в биохимических процессах, протекающих в живых организмах; катализаторами здесь являются ферменты. Ферменты — это сложные вещества белкового происхождения, обладающие узко специфическим каталитическим действием. Каждая из биохимических каталитических реакций имеет свой определенный фермент. Природой фермента будут определяться конкретные виды связей реагента в реакции. Примерами таких реакций, протекающих в нашем организме, могут служить ферментативные гидролизы углеводов, жиров, белков. Следует иметь в виду, что катализаторы чувствительны к ядам. Часто в каталитических реакциях используются специальные вещества — промоторы.
Промоторы — добавки, увеличивающие активность катализатора.
В разработку теории катализа и практику подбора и применения катализаторов большой вклад внес отечественный ученый Г.К. Боресков, основатель Института катализа РАН. Основные понятия Органические реакции как химические системы. Гомогенные и гетерогенные системы. Природа вещества. Реакционная способность. Энергия активации. Энергия органической реакции. Катализаторы. Ингибиторы. Виды катализа. Ферментативный катализ Вопросы и задания
|
|
|



 В обратимых реакциях катализатор в равной мере влияет на прямую и обратную реакции. Он не смещает химического равновесия, но, ускоряя цикл химических превращений, способствует более быстрому установлению равновесия. Ускорение реакции обусловлено тем, что катализатор, взаимодействуя с реагентами, образует промежуточные активные комплексы.
В обратимых реакциях катализатор в равной мере влияет на прямую и обратную реакции. Он не смещает химического равновесия, но, ускоряя цикл химических превращений, способствует более быстрому установлению равновесия. Ускорение реакции обусловлено тем, что катализатор, взаимодействуя с реагентами, образует промежуточные активные комплексы.
 1.Что такое химическая реакция, какие признаки и условия ее протекания вы знаете?
1.Что такое химическая реакция, какие признаки и условия ее протекания вы знаете?
 2. Каковы различия и взаимосвязи между понятиями «химические свойства» и «реакционная способность» соединений? Прокомментируйте это на конкретных примерах органических веществ.
2. Каковы различия и взаимосвязи между понятиями «химические свойства» и «реакционная способность» соединений? Прокомментируйте это на конкретных примерах органических веществ.
 3. Что такое тепловой эффект реакции? Приведите примеры термохимического уравнения экзотермической и эндотермической органических реакций.
3. Что такое тепловой эффект реакции? Приведите примеры термохимического уравнения экзотермической и эндотермической органических реакций.