|
|
|
|
|
Глава 4. Вещества в окружающей нас природе и в технике § 25. Массовая доля растворённого вещества
Растворы бывают концентрированные (с высоким содержанием растворённого вещества) и разбавленные (с низким содержанием растворённого вещества). Это качественная оценка концентрации растворов, применять которую можно весьма условно. Гораздо больший интерес представляют различные количественные способы выражения концентрации растворов. Концентрацию раствора часто выражают в массовых долях.
Например, если имеется 10%-й раствор поваренной соли ( Знание способов выражения концентрации очень важно для практического приготовления растворов и решения задач. Пример 1После полного упаривания 50 г раствора образовалось 6 г твёрдого остатка. Вычислите массовую долю растворённого вещества во взятом растворе.
Пример 2Необходимо приготовить 150 г 10 %-го раствора хлорида натрия, т. е. нужно найти, сколько для этой цели необходимо соли (г) и воды (мл).
Практически для приготовления раствора нужно отвесить на весах 15 г соли, отмерить мензуркой 135 мл воды (так как плотность воды равна единице), высыпать соль в воду и перемешать. Для приготовления неводного раствора определённой концентрации необходимо учитывать его плотность, пользуясь соотношением Основные понятия Массовая доля растворённого вещества Вопросы и задания
1) 0,2 г 2) 10 г 3) 12 г 4) 14 г
1) 3,4 % 2) 6,8 % 3) 8,5 % 4) 12,2 %
|
|
|



 Сколько вещества можно растворить в том или ином растворителе? Приведите примеры хорошо растворимых в воде веществ.
Сколько вещества можно растворить в том или ином растворителе? Приведите примеры хорошо растворимых в воде веществ.
 Массовой долей растворённого вещества (
Массовой долей растворённого вещества ( ) называют отношение массы растворённого вещества к общей массе раствора.
) называют отношение массы растворённого вещества к общей массе раствора.



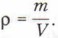
 1. Что такое массовая доля растворённого вещества?
1. Что такое массовая доля растворённого вещества?
 2. Чем различаются насыщенный раствор и концентрированный раствор?
2. Чем различаются насыщенный раствор и концентрированный раствор?
 4. В 500 г раствора, насыщенного при 20 °С, содержится 120 г нитрата калия KNO3 Найдите растворимость этой соли и массовую долю соли в растворе.
4. В 500 г раствора, насыщенного при 20 °С, содержится 120 г нитрата калия KNO3 Найдите растворимость этой соли и массовую долю соли в растворе.