|
|
|
|
|
Глава 5. Понятие о газах. Воздух. Кислород. Горение Законы Гей-Люссака и АвогадроПроведём некоторые простые расчёты на основании закона АвогадроI. Определение количества вещества в газе, занимающем известный объём при н. у., и определение объёма газа по известному количеству вещества Задача 1 (прямая)Определить количество вещества в газе, заполняющем при н. у. сосуд объёмом 11,2 л.
Задача 2 (обратная)Какой объём займёт углекислый газ количеством вещества 5 моль (н. у.)?
II. Объёмные соотношения газов при химических реакциях Для выполнения расчётов необходимо помнить, что коэффициенты в химических реакциях обозначают:
В случае газообразных веществ коэффициенты несут информацию об объёмных отношениях исходных веществ и продуктов реакции (при н. у.).
Задача 1Какой объём водорода (н. у.) потребуется для взаимодействия с азотом, масса которого 56 г? Каков объём образующегося при этом аммиака (н. у.)?
Задача 2Какой объём водорода (при н. у.) можно получить при взаимодействии 0,3 моль цинка с соляной кислотой?
Задача 3Определить объём (при н. у.) и массу водорода, который выделится при взаимодействии 1,95 г цинка с соляной кислотой.
Вопросы и задания
а) 3 моль; б) 0,4 моль; в) 2 моль; г) 400 моль?
С + O2 = CO2
2Na + 2Н2O = 2NaOH + Н2 ↑
а) при сгорании 3,2 г серы S + O2 = SO2; б) при затрате на сгорание серы 44,8 л кислорода; 2,24 л кислорода; 11,2 л кислорода.
|
|
|





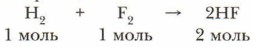




 1. Баллон вмещает 30 моль сжатого кислорода. Какой объём займёт этот газ при н. у.?
1. Баллон вмещает 30 моль сжатого кислорода. Какой объём займёт этот газ при н. у.?
 6. Рассчитайте объём (н. у.) сернистого газа SO2, образующегося:
6. Рассчитайте объём (н. у.) сернистого газа SO2, образующегося: