|
|
|
|
|
Глава 6. Основные классы неорганических соединений § 30. ОксидыИзучая химию, мы уже неоднократно встречались с различными классами неорганических соединений: оксидами, основаниями, кислотами, солями. Настало время расширить и систематизировать знания об этих значительных группах веществ. Выполним эту работу в два этапа. Сначала рассмотрим признаки состава соединений каждого класса, соответствующие им общие формулы и классификации, номенклатуры, а затем познакомимся с важнейшими общими химическими свойствами и способами получения соединений каждого класса. При изучении общих химических свойств основных классов неорганических соединений важно учитывать следующее: каждое вещество имеет индивидуальные свойства, присущие только ему. В то же время, являясь конкретным представителем определённого класса соединений, оно характеризуется свойствами, общими для всего этого класса. В последующих параграфах мы подробно познакомимся лишь с некоторыми особенно важными веществами: соляной и серной кислотами, едкими щелочами. В остальных случаях рассматривать индивидуальные свойства отдельных веществ мы не будем, а сосредоточим внимание на тех общих свойствах, которые характерны для всех представителей каждого класса соединений. Оксиды
Что вам известно об индикаторах? С какой целью их применяют? Задание. При изучении химических свойств кислорода мы познакомились с реакциями окисления и оксидами. На основании каких признаков в класс оксидов выделены следующие вещества?
Выберите из перечисленных формул веществ формулы оксидов: H2S, CaO, СO2, НСl, Н2O, Р2O5, Cu2O, NH3, НСlO, Fe2O3, SiO2. Итак, все оксиды по составу характеризуются тремя общими признаками: любой оксид является сложным веществом; состоит из атомов двух химических элементов; один из элементов — кислород. Все эти признаки могут быть выражены общей формулой, в которой Э — атомы химического элемента, образовавшего оксид; О — атомы кислорода; х, у — индексы, указывающие число атомов элементов, образующих оксид:
Оксидов много. Практически все простые вещества при окислении образуют оксиды. Атомы многих элементов, проявляя разные значения валентности, участвуют в образовании нескольких оксидов, например азоту соответствует пять веществ: N2O, NO, N2O3, NO2, N2O5. Познакомимся с физическими свойствами и классификацией оксидов. Начнём с выполнения лабораторных опытов.
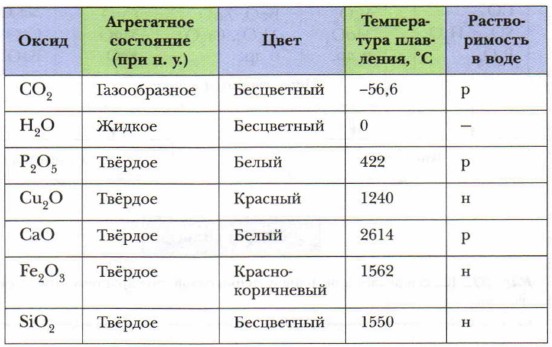
2. Поместите в пробирки с водой небольшие (размером меньше спичечной головки) порции оксида фосфора (V), оксида кремния (IV), оксида кальция и оксида железа (III). Размешайте стеклянными палочками. Что наблюдаете? Во все пробирки добавьте по 2-3 капли лакмуса. Результаты наблюдений и анализ данных таблицы позволяют сделать вывод о большом разнообразии физических свойств оксидов.
|
|
|



 Дайте определение оксидов и приведите их примеры.
Дайте определение оксидов и приведите их примеры.

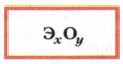
 1. Рассмотрите образцы перечисленных выше оксидов. Установите их агрегатное состояние и цвет, используя таблицу.
1. Рассмотрите образцы перечисленных выше оксидов. Установите их агрегатное состояние и цвет, используя таблицу.