|
|
|
|
|
Глава 9. Строение вещества Степень окисленияМногие элементы, и особенно элементы побочных подгрупп, имеют переменную степень окисления. Так, например, марганец имеет степень окисления в разных его соединениях +2, +3, +4, +6, +7:
Степень окисления тесно связана с ОЭО элемента и также обусловлена его местом в периодической системе Д.И. Менделеева. В природе элементы встречаются в соединениях, где проявляют характерную и устойчивую степень окисления. Так, у кислорода такой устойчивой степеныо окисления является -2, но в соединении с более электроотрицательным элементом фтором он имеет положительную степень окисления В свободных состояниях
Степень окисления не следует отождествлять с валентностью элементов. Валентность — это реальное свойство атомов, которое проявляется в их способности образовывать химические связи с другими атомами. Валентность в ковалентном соединении измеряется числом химических двухэлектронных связей или числом связывающих электронных пар. Так, молекула O2 образована двумя ковалентными связями O = O, валентность кислорода в данном веществе равна II, а степень окисления равна нулю. Молекула азота образована с помощью трёх ковалентных связей N ≡ N, следовательно, азот здесь трёхвалентный. В большинстве случаев численные значения валентности и степени окисления элементов в соединениях совпадают, но не во всех случаях они численно равны. Например, в пероксиде водорода Понятие валентности применимо лишь к ковалентным соединениям, как простым, так и сложным:
Степень окисления характеризует состояние атомов элементов только в сложном веществе, причём как с ковалентными, так и с ионными связями их атомов. В дальнейшем это понятие будет необходимо для составления уравнений окислительно-восстановительных реакций. Основные понятия Степень окисления • Определение степени окисления элементов в соединениях Вопросы и задания
|
|
|



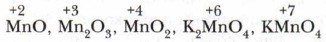
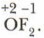
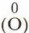 и в простых веществах
и в простых веществах 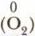 степень окисления элементов равна нулю, так как их валентные электроны не смещены.
степень окисления элементов равна нулю, так как их валентные электроны не смещены.

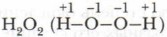 степень окисления кислорода равна -1, так как от водорода к атому кислорода оттягивается лишь один электрон, а у атомов кислорода одинаковая ОЭО.
степень окисления кислорода равна -1, так как от водорода к атому кислорода оттягивается лишь один электрон, а у атомов кислорода одинаковая ОЭО.
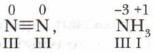
 1. Сформулируйте определение степени окисления. Для чего и кем введена в науку эта характеристика элемента?
1. Сформулируйте определение степени окисления. Для чего и кем введена в науку эта характеристика элемента?
 5. Каковы значения степени окисления и валентности элементов в веществах, формулы которых: Н2O2, Na2O2, FeS2? Объясните их смысл.
5. Каковы значения степени окисления и валентности элементов в веществах, формулы которых: Н2O2, Na2O2, FeS2? Объясните их смысл.