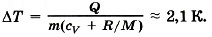|
|
|
|
|
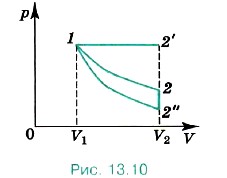
Глава 13. Основы термодинамики § 80. Примеры решения задач по теме: Первый закон термодинамикиВ большей части задач используется не общая форма первого закона термодинамики, а его различные частные формулировки, применимые к определённым процессам. Задачи на теплообмен в изолированной системе решаются с помощью уравнения теплового баланса (13.10). При решении задач надо чётко выделять начальное и конечное состояния системы, а также характеризующие её параметры. Задача 1. Во время расширения газа, вызванного его нагреванием, в цилиндре с площадью поперечного сечения S = 200 см2 газу было передано количество теплоты Q = 1,5 • 105 Дж, причём давление газа оставалось постоянным и равным р = 2 • 107 Па. На сколько изменилась внутренняя энергия газа, если поршень передвинулся на расстояние Δh = 30 см? Р е ш е н и е. Согласно первому закону термодинамики в форме (13.12) Q = ΔU + А', где А' = pSΔh — работа, совершённая газом. Отсюда ΔU = Q - pSΔh = 30 кДж. Задача 2. Газ расширяется от объёма V1 до объёма V2 один раз изотермически, другой изобарно и третий адиабатно. При каком процессе газ совершает большую работу и при каком газу передаётся большее количество теплоты? Р е ш е н и е. На диаграмме р—V (рис. 13.10) изобразим все три процесса. Работа численно равна площади криволинейной трапеции. Из рисунка очевидно, что работа при изобарном процессе будет максимальной, при адиабатном минимальной, т. е. A'1 - 2' > A'1—2 > A1—2".
Температура газа в состоянии 2' больше, чем в состоянии 2, а температура в состоянии 2 больше, чем в состоянии 2" (Т2' > Т2 > Т2"). В этом легко убедиться, начертив изотермы, проходящие через точки 2' и 2". При процессе 1—2' изменение внутренней энергии AU > 0, при процессе 1—2 ΔU = 0. Очевидно, что поскольку Q = ΔU + А' (первый закон термодинамики), то Q1-2' > Q2 - 2 > Q1- 2" (Q1 - 2" = 0). Задача 3. Пусть азот нагревается при постоянном давлении. Зная, что масса азота m = 280 г, количество затраченной теплоты Q = 600 Дж и удельная теплоёмкость азота при постоянном объёме cv = 745 Дж/(кг • К), определите, на сколько повысилась температура азота. Молярная масса азота М = 0,028 кг/моль. Р е ш е н и е. Согласно первому закону термодинамики Q = ΔU + А'. Изменение внутренней энергии ΔU = cvmΔT. Работа при изобарном процессе А' = pΔV = (m/M)RΔT. Следовательно, Q = mΔT(cv + R/M), откуда
|
|
|