|
|
|
|
|
Глава 6. Свойства газов § 33. Насыщенный парПарообразование1. Процесс перехода вещества из жидкого состояния в газообразное называют парообразованием. Парообразование осуществляется при испарении и при кипении. Вспомним, как происходит испарение. Молекулы жидкости, участвующие в тепловом движении, удерживают друг около друга действующие между ними силы притяжения. Однако есть молекулы жидкости, кинетическая энергия которых достаточно велика и превосходит потенциальную энергию их взаимодействия. Такие молекулы могут совершить работу по преодолению сил притяжения (работу выхода) и покинуть жидкость. Молекулы, вылетевшие из жидкости, беспорядочно движутся, некоторые из них в результате столкновений могут приобрести соответствующую скорость и вернуться в жидкость. Однако таких молекул мало, большинство молекул рассеиваются в окружающем пространстве, если сосуд, из которого они вылетают, открыт. Над жидкостью в этом случае находится ненасыщенный пар. Испарение будет происходить до тех пор, пока вся жидкость не превратится в пар. Насыщенный пар2. Пусть теперь жидкость находится в закрытом сосуде. В этом случае молекулы, вылетевшие из жидкости, уже не будут рассеиваться в атмосфере. Часть молекул возвратится в жидкость. В начале процесса испарения число молекул, вылетевших из жидкости, будет больше, чем число молекул, вернувшихся в неё. Поэтому плотность пара будет постепенно возрастать. При этом число молекул, возвращающихся в жидкость, тоже будет постепенно увеличиваться. Настанет такой момент, когда число молекул, вылетевших из жидкости, будет равно числу молекул, возвращающихся обратно в жидкость. Теперь число молекул над жидкостью и соответственно плотность пара изменяться не будут. Говорят, что в этом случае существует динамическое равновесие между паром и жидкостью и пар является насыщенным.
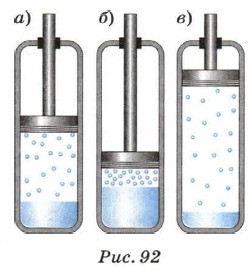
Свойства насыщенного пара3. Рассмотрим, какими свойствами обладает насыщенный пар. Пусть в цилиндре под поршнем находятся жидкость и её насыщенный пар (рис. 92, а). Будем опускать поршень, при этом объём пара уменьшится, а плотность и давление в первый момент возрастут. Это приведёт к нарушению равновесия между паром и жидкостью: число молекул, возвращающихся в жидкость, станет больше, чем число молекул, покидающих её (рис. 92, б). Число молекул пара уменьшится, и восстановится прежнее давление. Это можно пояснить, используя уравнение состояния газа: р = nkТ или
|
|
|



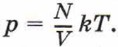 Если одновременно в одно и то же число раз изменяются число молекул газа и его объём, то давление при постоянной температуре остаётся неизменным.
Если одновременно в одно и то же число раз изменяются число молекул газа и его объём, то давление при постоянной температуре остаётся неизменным.