|
|
|
|
|
Глава 12. Твёрдые тела § 72. Кристаллические и аморфные телаМы живём на поверхности твёрдого тела — земного шара, в домах, построенных из твёрдых тел. Различные приборы, орудия труда сделаны из твёрдых тел. Знать свойства твёрдых тел необходимо. Вспомните, что такое твёрдое тело. Чем мы пренебрегали, когда в механике считали, что тело абсолютно твёрдое? Каковы физические свойства твёрдых тел? Какие физические величины характеризуют свойства твёрдых тел? Твёрдые тела сохраняют не только свой объём, как жидкости, но и форму. Они находятся преимущественно в кристаллическом состоянии.
Поэтому кристаллы имеют плоские грани. Например, крупинка обычной поваренной соли имеет плоские грани, составляющие друг с другом прямые углы (рис. 12.1). Это можно заметить, рассматривая соль с помощью лупы. А как геометрически правильна форма снежинки! В ней также отражена геометрическая правильность внутреннего строения кристаллического твёрдого тела — льда (рис. 12.2). Анизотропия кристаллов. Однако правильная внешняя форма не единственное и даже не самое главное следствие упорядоченного строения кристалла.
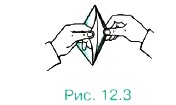
Прежде всего бросается в глаза различная механическая прочность кристаллов по разным направлениям. Например, кусок слюды легко расслаивается в одном из направлений на тонкие пластинки (рис. 12.3), но разорвать его в направлении, перпендикулярном пластинкам, гораздо труднее. Так же легко расслаивается в одном направлении кристалл графита.
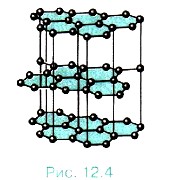
Это происходит потому, что кристаллическая решётка графита имеет слоистую структуру. Слои образованы рядом параллельных сеток, состоящих из атомов углерода (рис. 12.4). Атомы располагаются в вершинах правильных шестиугольников. Расстояние между слоями сравнительно велико — примерно в 2 раза больше, чем длина стороны шестиугольника, поэтому связи между слоями менее прочны, чем связи внутри их. Многие кристаллы по-разному проводят тепло и электрический ток в различных направлениях. От направления зависят и оптические свойства кристаллов. Все кристаллические тела анизотропны. Монокристаллы и поликристаллы. Кристаллическую структуру имеют металлы.
Если взять сравнительно большой кусок металла, то на первый взгляд его кристаллическое строение никак не проявляется ни во внешнем виде этого куска, ни в его физических свойствах. Металлы в обычном состоянии не обнаруживают анизотропии. Дело здесь в том, что обычно металл состоит из огромного количества сросшихся друг с другом маленьких кристалликов. Под микроскопом или даже с помощью лупы их нетрудно рассмотреть, особенно на свежем изломе металла (рис. 12.5). Свойства каждого кристаллика зависят от направления, но кристаллики ориентированы по отношению друг к другу беспорядочно. В результате в объёме, значительно превышающем объём отдельных кристалликов, все направления внутри металлов равноправны и свойства металлов одинаковы по всем направлениям.
В обычных условиях поликристаллическое тело образуется в результате того, что начавшийся рост многих кристаллов продолжается до тех пор, пока они не приходят в соприкосновение друг с другом, образуя единое тело. К поликристаллам относятся не только металлы. Кусок сахара, например, также имеет поликристаллическую структуру.
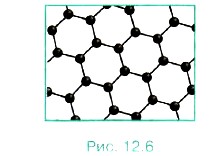
Мы говорили только о трёхмерных кристаллах. В 2004 г. был получен графен — двумерный кристалл, состоящий из одиночного слоя атомов углерода и имеющий идеальную гексагональную решётку (рис. 12.6). В 30-х годах прошлого века было доказано, что двумерные кристаллы неустойчивы и легко разрушаются. Однако графен имеет волнообразную структуру, что определяет его устойчивость. Графен обладает уникальными свойствами — он прочен, имеет высокую проводимость и прозрачен. Из него можно собрать трёхмерный кристалл графита.
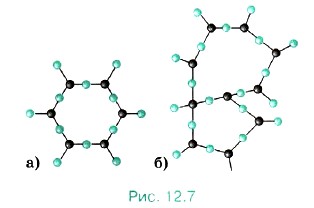
Аморфные тела. Кроме твёрдых тел, имеющих кристаллическую структуру, которая характеризуется строгим порядком в расположении атомов, существуют аморфные твёрдые тела. У аморфных тел нет строгого порядка в расположении атомов. Только ближайшие атомы-соседи располагаются в некотором порядке. Но строгой повторяемости по всем направлениям одного и того же элемента структуры, которая характерна для кристаллов, в аморфных телах нет. По расположению атомов и по их поведению аморфные тела аналогичны жидкостям. Часто одно и то же вещество может находиться как в кристаллическом, так и в аморфном состоянии. Например, кварц Si02 может быть как в кристаллической, так и в аморфной форме (кремнезём). Кристаллическую форму кварца схематически можно представить в виде решётки из правильных шестиугольников (рис. 12.7, а). Аморфная структура кварца также имеет вид решётки, но неправильной формы. Наряду с шестиугольниками в ней встречаются пяти- и семиугольники (рис. 12.7, б).
|
|
|




 Когда вы пишете карандашом, такое расслоение графита происходит непрерывно и его тонкие слои остаются на бумаге.
Когда вы пишете карандашом, такое расслоение графита происходит непрерывно и его тонкие слои остаются на бумаге.

 Растворите в стакане с водой соль, сделайте концентрированный раствор. Опустите в насыщенный раствор несколько кристалликов соли и оставьте, пока вся вода не испарится. Посмотрите, что останется в стакане. Сделайте выводы.
Растворите в стакане с водой соль, сделайте концентрированный раствор. Опустите в насыщенный раствор несколько кристалликов соли и оставьте, пока вся вода не испарится. Посмотрите, что останется в стакане. Сделайте выводы.