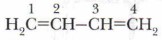|
|
|
|
|
Глава 5. Углеводороды § 13. Алкадиены. Строение, свойства, применение
Алкадиены, или диеновые углеводороды, имеют две двойные связи. Их общая формула CnH2n-2. Две двойные связи в молекуле углеводорода могут располагаться различным образом: а) две двойные связи сосредоточены у одного атома углерода — кумулированные связи:
б) две двойные связи разделены одной простой связью — сопряжённые связи:
в) две двойные связи разделены двумя и более простыми связями — изолированные связи:
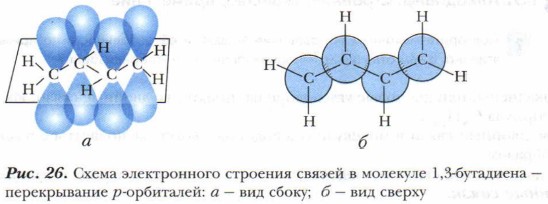
Наиболее важными соединениями являются алкадиены с сопряжёнными двойными связями. Каждый атом углерода находится в состоянии sр2-гибридизации. Это означает, что у всех атомов углерода имеется по одной негибридизированной 2р-орбитали (рис. 26, см. также рис. 8).
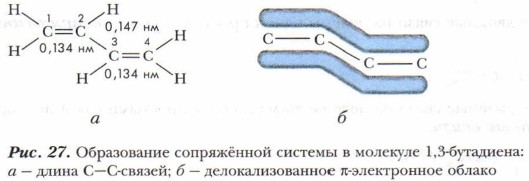
2р-орбиталь атома С1 перекрывается с 2р-орбиталью атома С2, а 2р-орбиталь атома С3 перекрывается с 2р-орбиталью атома С4. Однако и 2р-орбитали атомов С2 и С3 также перекрываются между собой, правда, это перекрывание несколько меньше, чем перекрывание между атомами С1 и С2 и перекрывание между атомами С3 и С4. В результате образуется единое π-электронное облако, распределённое по всей молекуле, создаётся система сопряжённых связей (рис. 27), которую можно представить в виде схемы.
В сопряжённой системе π-электроны делокализованы по всем атомам в молекуле (не имеют определённого места), т. е. происходит выравнивание длин связей: двойная связь (0,134 нм) несколько длиннее, чем в этилене, а одинарная (0,147 нм) короче, чем в алканах. Система становится более устойчивой. Это состояние получило название эффекта сопряжения, или р-π-сопряжения.
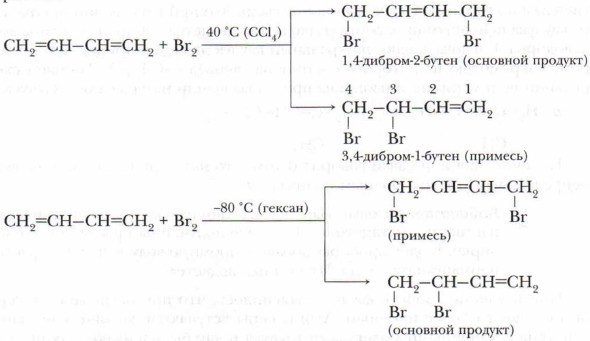
Наибольшее значение из различных представителей диеновых углеводородов имеют 1,3-бутадиен и 2-метил-1,3-бутадиен (изопрен), т. е. алкадиены с сопряженными двойными связями: Физические свойства. 1,3-Бутадиен при обычных условиях — газ, легко сжижается при температуре -5 °С. 2-метил-1,3-бутадиен — легкокипящая летучая жидкость, температура кипения +34,1 °С. Задание. Учитывая, что алкадиены имеют две двойные связи, предположите, какие реакции будут характерны для них. Химические свойства. Сопряжённые алкадиены как типичные представители непредельных углеводородов вступают в реакции присоединения. А. Галогенирование Присоединение диенами галогенов протекает с образованием смеси продуктов присоединения в 1,2- и 1,4-положениях. Соотношение продуктов зависит от конкретных условий, например температуры реакции и природы растворителя:
Задание. Запишите уравнение реакции взаимодействия 1,3-бута- диена с избытком водорода.
|
|
|



 Повторите механизм образования π-связи и её особенности на примере этилена. В чём отличие sр2-гибридизации от sр3-гибридизации?
Повторите механизм образования π-связи и её особенности на примере этилена. В чём отличие sр2-гибридизации от sр3-гибридизации?
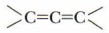
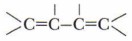
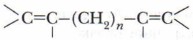
 Рассмотрим электронное строение этих углеводородов на примере молекулы 1,3-бутадиена, или дивинила:
Рассмотрим электронное строение этих углеводородов на примере молекулы 1,3-бутадиена, или дивинила: