|
|
|
|
|
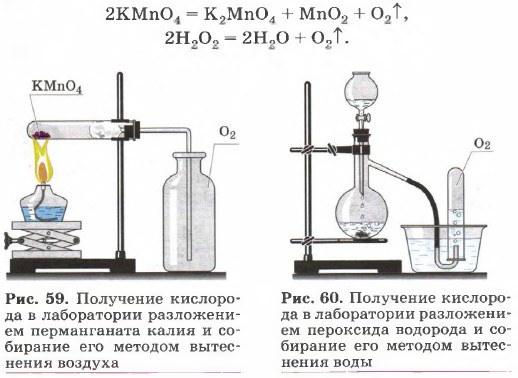
Глава первая. Углеводороды и их природные источники § 8. Газообразные вещества (продолжение)В лаборатории кислород получают разложением перманганата калия (рис. 59) или пероксида водорода (рис. 60):
Собирают кислород в сосуд методом вытеснения воздуха (см. рис. 59), так как он немного тяжелее воздуха, или методом вытеснения воды (см. рис. 60), так как он в ней малорастворим.
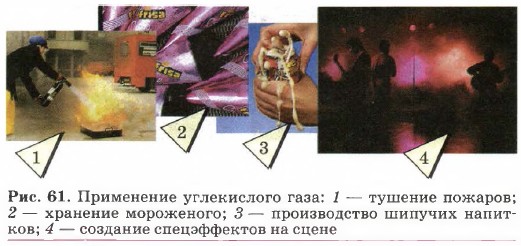
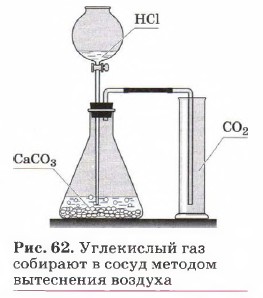
Распознать кислород можно по вспыхиванию внесённой в пробирку с этим газом тлеющей лучинки. Углекислый газ СO2 широко применяют для изготовления шипучих напитков, тушения пожаров и получения «сухого льда», который используют для охлаждения и хранения продуктов питания, в первую очередь мороженого (рис. 61). В промышленности углекислый газ получают обжигом известняка: СаСO3 = СаО + СO2↑. В лаборатории оксид углерода (IV) получают действием соляной кислоты на мрамор: CaCOg + 2НСl = СаСl2 + Н2O + СO2↑. Собирают углекислый газ в сосуд методом вытеснения воздуха, так как оксид углерода (IV) почти в 1,5 раза тяжелее его (рис. 62).
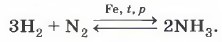
Распознать углекислый газ можно или с помощью горящей лучинки, которая гаснет в его атмосфере (углекислый газ не поддерживает горение) (рис. 63, а), или по помутнению известковой воды (рис. 63, б): СO2 + Ca(OH)2 = CaCO3↓ + Н2O. Из воздуха получают не только кислород, но и азот, который вместе с водородом служит сырьём для получения ценного газообразного продукта — аммиака NH3:
В лаборатории аммиак получают взаимодействием щелочей с солями аммония (рис. 64): 2NH4Cl + Са(ОН)2 = СаСl2 + 2Н2O + 2NH3↑.
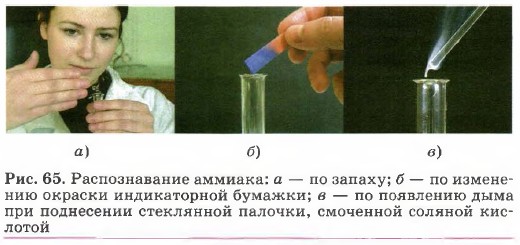
Аммиак легче воздуха, поэтому его собирают методом вытеснения воздуха в перевёрнутый вверх дном сосуд. Распознать аммиак можно: а) по запаху; б) по изменению окраски влажной лакмусовой бумажки (с красного цвета на синий); в) по появлению дыма при поднесении стеклянной палочки, смоченной соляной кислотой (рис. 65). Природный газ служит сырьём для получения ценных газообразных органических соединений, например этилена.
|
|
|