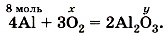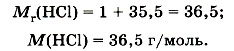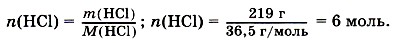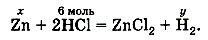|
|
|
|
|
Глава четвёртая. Изменения, происходящие с веществами Расчёты по химическим уравнениям3. Над формулой алюминия в уравнении реакции запишем найденное количество — 8 моль, а количества кислорода и оксида алюминия обозначим соответственно через х и у:
4. Согласно уравнению реакции 4 моль алюминия взаимодействует с 3 моль кислорода, в результате чего получается 2 моль оксида алюминия. Следовательно, 8 моль алюминия соответствуют 6 моль кислорода и 4 моль оксида алюминия. п(O2) = 6 моль; n(Аl2O3) = 4 моль. 5. Рассчитаем объём кислорода по найденному количеству вещества: V(O2) = n(O2) • Vm; V(O2) = 6 моль • 22,4 л/моль = 134,4 л. 6. Однако в задаче требуется найти объём не кислорода, а воздуха. В воздухе содержится 21% кислорода по объёму. Преобразуя формулу φ = V(O2)/V(возд), найдём объём воздуха: V(возд) = V(O2) : φ(O2) = 134,4 : 0,21 = 640 (л). Ответ: V(возд) = 640 л; n(Аl2O3) = 4 моль.
б) Найдём молярную массу хлороводорода:
Рассчитаем количество вещества хлороводорода:
3. Над формулой хлороводорода в уравнении реакции запишем найденное количество вещества — 6 моль, а количество веществ цинка и водорода обозначим соответственно через х и у:
4. Согласно уравнению реакции 2 моль хлороводорода взаимодействует с 1 моль цинка, в результате чего получается 1 моль водорода. Следовательно, 6 моль хлороводорода соответствуют 3 моль цинка и 3 моль водорода. 5. Рассчитаем объём водорода по найденному количеству:
1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания. 2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и слово-сочетаниям следующего параграфа.
1. Какой объём водорода (н. у.) и количество вещества соли образуется при взаимодействии соляной кислоты с 540 мг алюминия, содержащего 4 % примесей? 2. Какая масса оксида кальция получится при разложении 250 кг карбоната кальция, содержащего 20% примесей? Какой объём (н. у.) оксида углерода (IV) при этом выделится? 3. Сколько молекул кислорода и какой объём водорода (н. у.) образуется при разложении 180 г воды? 4. Придумайте условие задачи, в которой необходимо использовать приведённое ниже уравнение, и решите её: Н3РO4 + 3NaOH = Na3PO4 + 3H2O. 5. Придумайте и решите задачу, в условиях которой была бы дана масса раствора вещества с определённой массовой долей растворённого вещества, а требовалось бы найти количество вещества одного из веществ и объём другого. При составлении задачи используйте уравнение реакции: Zn + H2SO4 = ZnSO4 + Н2. <<< К началу Ответы к § 29 >>>
|
|
|