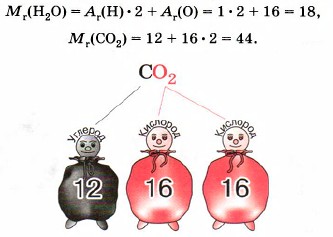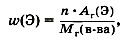|
|
|
|
|
Введение Химические формулы. Относительная атомная и молекулярная массыЧтобы узнать относительную молекулярную массу вещества, не обязательно делить массу его молекулы на массу атома водорода. Нужно просто сложить относительные атомные массы элементов, образующих вещество, с учётом числа атомов, например:
Химическая формула содержит важную информацию о веществе. Например, формула СО2 показывает следующую информацию: 1. Конкретное вещество — углекислый газ. 2. Качественный состав — состоит из двух элементов: углерода и кислорода. 3. Тип вещества — сложное вещество. 4. Количественный состав вещества — в молекуле содержится 1 атом углерода и 2 атома кислорода. 5. Относительную молекулярную массу — Мr(СО2) = = 12 + 16×2 = 44. 6. Соотношение масс элементов в этом веществе: m(С): m{О) = 12 : 32 = 1 : 2,6. 7. Массовые доли элементов в этом веществе, которые рассчитывают по формуле:
где ω (Э) — массовая доля элемента Э в веществе; n — число атомов элемента Э в веществе; Аr(Э) — относительная атомная масса элемента Э; Мr(в-ва) — относительная молекулярная масса вещества. Рассчитаем массовые доли элементов углерода и кислорода в углекислом газе СО2.
1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания. 2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
1. Что означают записи: ЗН; 2Н2О2? 2. Запишите формулу сахарозы, если известно, что в состав её молекулы входят двенадцать атомов углерода, двадцать два атома водорода и одиннадцать атомов кислорода. 3. Используя рисунок 2 (см. с. 5), запишите формулы веществ и рассчитайте их относительные молекулярные массы. 4. Какой форме существования химического элемента кислорода соответствует каждая из следующих записей: 3О2; 4СО2? 5. Почему относительная атомная масса элемента и относительная молекулярная масса вещества не имеют единиц измерения? 6. В каком из веществ, формулы которых SО2 и SО3, массовая доля серы больше? Ответ подтвердите расчётами. 7. Вычислите массовые доли элементов в азотной кислоте HNO3. 8. Дайте полную характеристику глюкозы С6Н12O6, используя пример описания углекислого газа СО2 (см. с. 42).
|
|
|