|
|
|
|
|
Глава 2. Химические реакции. Законы сохранения массы и энергии Сущность, признаки и условия протекания химических реакций. Тепловой эффект химической реакции
Количество выделенной (или поглощённой) теплоты называют тепловым эффектом реакции. Тепловой эффект обычно обозначают буквой Q и соответствующим знаком: +Q — для экзотермических реакций и -Q — для эндотермических реакций. Область химии, занимающаяся изучением тепловых эффектов химических реакций, называется термохимией. Уравнения химических реакций, в которых указан тепловой эффект, называют термохимическими. Ранние исследования термохимических явлений принадлежат учёному Н.Н. Бекетову. Значение теплового эффекта относят к 1 моль вещества и выражают в килоджоулях.
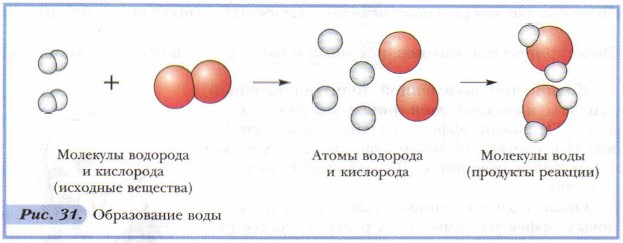
Попробуем объяснить, в чём сущность происходящих превращений веществ и что происходит с атомами реагирующих веществ. Согласно атомномолекулярному учению все вещества состоят из атомов, соединённых друг с другом в молекулы или другие частицы. В процессе реакции происходит разрушение исходных веществ (реагентов) и образование новых веществ (продуктов реакции). Таким образом, все реакции сводятся к образованию новых веществ из атомов, входящих в состав исходных веществ. Следовательно, сущность химической реакции состоит в перегруппировке атомов, в результате которой из молекул (или других частиц) получаются новые молекулы (или другие формы вещества). Процесс перегруппировки атомов в ходе химической реакции можно представить с помощью графических моделей, изображённых на рисунке 31.
Основные понятия Химическая реакция • Признаки и условия возникновения и течения реакций • Экзотермические и эндотермические реакции • Тепловой эффект • Термохимическое уравнение Вопросы и задания
Объясните её с точки зрения атомно-молекулярного учения.
|
|
|




 Что происходит с веществами в процессе химической реакции?
Что происходит с веществами в процессе химической реакции?
 Химической реакцией называют превращение одних веществ в другие. Вещества, полученные в результате реакции, отличаются от исходных веществ составом, строением и свойствами.
Химической реакцией называют превращение одних веществ в другие. Вещества, полученные в результате реакции, отличаются от исходных веществ составом, строением и свойствами.
 1. Что называется химической реакцией?
1. Что называется химической реакцией?
 3. Какие признаки говорят о том, что перечисленные ниже процессы являются химическими реакциями: а) гниение листьев; б) пригорание пищи; в) ржавление железа; г) окисление меди; д) взаимодействие известковой воды и углекислого газа; е) скисание молока?
3. Какие признаки говорят о том, что перечисленные ниже процессы являются химическими реакциями: а) гниение листьев; б) пригорание пищи; в) ржавление железа; г) окисление меди; д) взаимодействие известковой воды и углекислого газа; е) скисание молока?
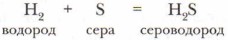
 6. К какому типу — экзо- или эндотермическому — относятся следующие реакции: образование воды из водорода и кислорода, самовозгорание и взрыв метана (газ, который часто выделяется породой и скапливается в шахтах).
6. К какому типу — экзо- или эндотермическому — относятся следующие реакции: образование воды из водорода и кислорода, самовозгорание и взрыв метана (газ, который часто выделяется породой и скапливается в шахтах).

 7. Предложите и с помощью компьютера начертите схему прибора для измерения теплового эффекта химической реакции. Обсудите её с товарищем.
7. Предложите и с помощью компьютера начертите схему прибора для измерения теплового эффекта химической реакции. Обсудите её с товарищем.