|
|
|
|
|
Глава 5. Понятие о газах. Воздух. Кислород. Горение § 29. Химические свойства и применение кислорода
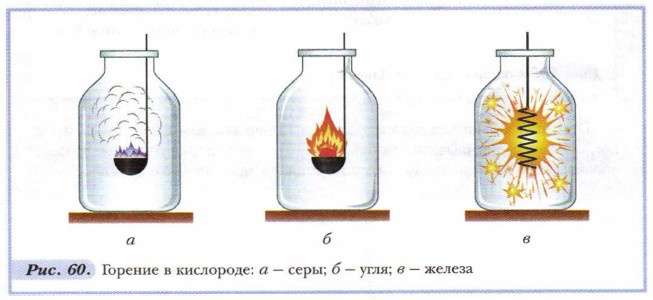
Под химическими свойствами понимают совокупность химических реакций, в которые вступает вещество. Мы уже знаем, что реакции горения особенно интенсивно протекают в атмосфере кислорода. Например, тлеющая лучинка вспыхивает, если её внести в сосуд, наполненный этим газом. Попробуем провести реакции взаимодействия серы и углерода с кислородом. Для этого возьмём ложечкой для сжигания веществ по кусочку серы и угля и внесём в сосуды, наполненные кислородом. Никаких видимых изменений не происходит. Вы уже знаете, что для возникновения химического взаимодействия, помимо введения веществ в соприкосновение, нередко требуется их предварительное нагревание. Нагреем кусочек серы до воспламенения. Сера горит красивым голубым пламенем, от неё струится «белый дымок» — это оксид серы (IV) SO2 (сернистый газ), образовавшийся в результате взаимодействия серы и кислорода, — продукт реакции. Вскоре появится удушливый запах этого вещества, поэтому опыт следует проводить в вытяжном шкафу. Внесём горящую серу в сосуд с кислородом. Пламя преобразилось: оно стало значительно больше и ярче. Сера быстро догорает с образованием сернистого газа (рис. 60, а). Повторим этот опыт с кусочком угля, а затем с металлами. Уголь на воздухе придётся накалить докрасна. После помещения его в атмосферу кислорода он быстро сгорит. Продукт реакции — углекислый газ (рис. 60, б). Медь и железо — металлы, которые при нагревании на воздухе не загораются. Сильно нагреем стальную (железо) стружку и поместим в банку с кислородом. Затраченные на длительное нагревание усилия не пропадут даром: мы сможем полюбоваться ослепительным фейерверком искр, которые образуются при взаимодействии кислорода с железом (рис. 60, в).
Разобраться в сущности процессов, которые происходили в наблюдаемых опытах, помогут уравнения химических реакций:
Сравните уравнения проведённых химических реакций. В результате этого вы должны прийти к следующим выводам. 1. В реакции взаимодействия с кислородом вступают простые вещества: металлы и неметаллы. 2. Одно из обязательных условий начала реакции — предварительное нагревание веществ. 3. Интенсивность протекания реакций резко увеличивается в атмосфере кислорода. 4. Все реакции взаимодействия с кислородом простых веществ относятся к реакциям соединения. Рассмотренные примеры позволяют нам несколько углубить и расширить имеющиеся знания:
|
|
|



 Какие явления называют химическими? Каковы условия возникновения и протекания химических реакций?
Какие явления называют химическими? Каковы условия возникновения и протекания химических реакций?
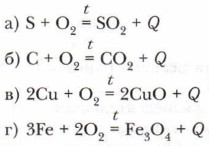
 а) реакции взаимодействия веществ с кислородом называются реакциями окисления;
а) реакции взаимодействия веществ с кислородом называются реакциями окисления;