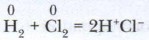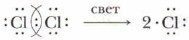|
|
|
|
|
Глава 12. Галогены Хлороводород, соляная кислота и их свойств
Определите степень окисления хлора в этом соединении. Определите вид химической связи в молекуле хлороводорода. ХлороводородСреди галогеноводородов особое значение имеет хлороводород. Получение хлороводорода. В лаборатории хлороводород можно получить нагреванием твёрдого хлорида натрия с концентрированной серной кислотой:
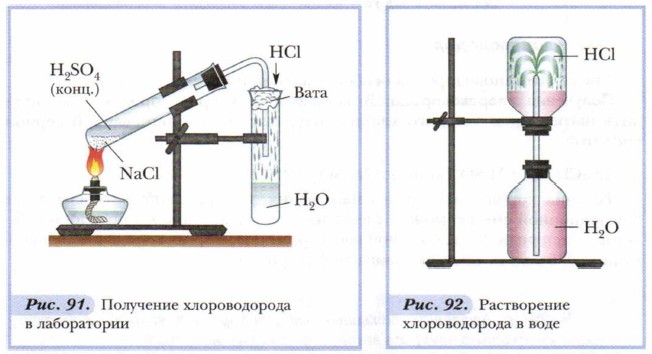
Реакция хорошо идёт и без нагревания, но при необходимости сосуд с реакционной смесью можно слегка нагреть, выделение хлороводорода будет интенсивным. Из-за большой растворимости хлороводорода в воде необходимо соблюдать технику безопасности (рис. 91)!
Физические свойства хлороводорода. Хлороводород — бесцветный газ, немного тяжелее воздуха, с резким запахом, дымит во влажном воздухе. Хлороводород относится к числу наиболее растворимых в воде газообразных веществ. В 1 л воды при комнатной температуре может раствориться до 500 л хлороводорода (рис. 92). Раствор хлороводорода в воде называют хлороводородной (соляной) кислотой. Основное применение хлороводорода — получение соляной кислоты.
|
|
|



 Запишите молекулярную и электронную формулы хлороводорода.
Запишите молекулярную и электронную формулы хлороводорода.