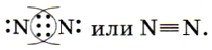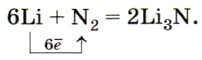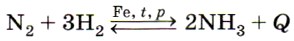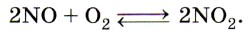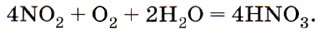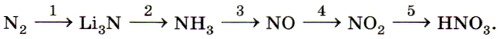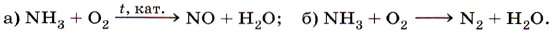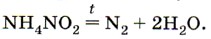|
|
|
|
|
Глава 3. Неметаллы § 28. Азот
Строение и свойства атомов. Элемент азот N — первый представитель главной подгруппы V группы Периодической системы Д. И. Менделеева. Его атомы содержат на внешнем энергетическом уровне пять электронов, из которых три электрона неспаренные (вспомните правило «8 - N», где N — число электронов на внешнем энергетическом уровне). Отсюда следует, что атомы этого элемента могут присоединять три электрона, завершая внешний энергетический уровень, и вследствие этого приобретают степень окисления -3, например в соединениях с водородом — аммиаке NH3 и с металлами — нитридах Li3N, Mg3N2 и др. Атомы азота могут также отдавать свои внешние электроны более электроотрицательным элементам (фтору, кислороду) и приобретать при этом степени окисления +3 и +5. Атомы азота в степенях окисления + 1, +2, +3, +4 могут проявлять как окислительные, так и восстановительные свойства. Азот — простое вещество. В свободном состоянии азот существует в виде двухатомных молекул N2. В молекуле N2 атомы азота связаны отличающейся высокой прочностью тройной ковалентной связью.
Азот — бесцветный газ без запаха и вкуса. В воде растворяется хуже кислорода. Прочностью молекулы азота обусловлена его химическая инертность. При обычных условиях азот взаимодействует только с литием, образуя нитрид лития Li3N:
С другими металлами он взаимодействует только при высоких температурах. Также при высоких температурах, давлении и в присутствии катализатора азот реагирует с водородом, образуя аммиак:
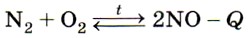
(дайте характеристику этой реакции по всем изученным вами признакам классификации реакций). При температуре электрической дуги он соединяется с кислородом, образуя оксид азота (II):
(дайте характеристику этой реакции по всем изученным вами признакам классификации реакций). В природе подобный процесс наблюдается при грозах (рис. 125).
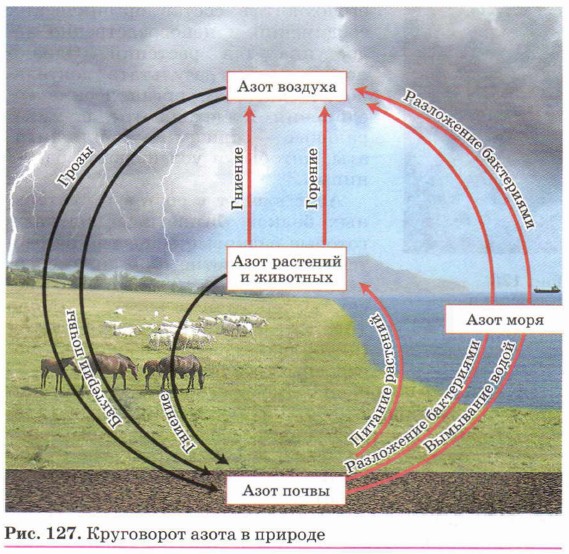
В природе азот содержится в основном в атмосфере — 78,08% по объёму или 75,51% по массе. Над каждым гектаром земной поверхности постоянно «висит» 8000 т азота. Из природных неорганических соединений азота наиболее известна чилийская селитра NaN03. Она образовалась из остатков птичьего помёта в условиях сухого и жаркого климата. Редко выпадающие осадки смывали образующуюся селитру в ложбины, в которых со временем и накопились немалые её запасы. На многочисленных птичьих базарах российского Севера процесс превращения птичьего помёта в селитру невозможен (почему?). Большая часть связанного азота содержится в органических веществах. Азот, полученный перегонкой жидкого воздуха, в промышленности применяют для синтеза аммиака и производства азотной кислоты. Раньше этот газ в качестве инертной среды использовали для наполнения электрических ламп. В медицине чистый азот применяют в качестве инертной среды при лечении туберкулёза лёгких, а жидкий азот — при лечении заболеваний позвоночника, суставов и др. Круговорот азота в природе. Азот — жизненно важный элемент. Все основные части клеток тканей организма построены из белковых молекул, в состав которых входит азот. Без белка нет жизни, а без азота нет белка. Человек получает белки из растительной и животной пищи, животные, в свою очередь, получают их также из растений. Следовательно, растения — один из источников пополнения азота, который поддерживает жизнь. Содержание связанного азота в почве очень незначительно (до 1 кг в 1 т), к тому же большая часть
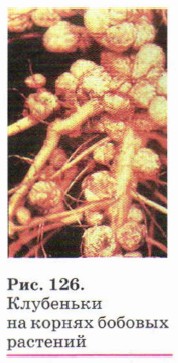
его входит в состав органических соединений и непосредственно недоступна для растений. Однако постепенно, в результате деятельности бактерий, органические соединения превращаются в минеральные — соли аммония или нитраты, которые и усваиваются растениями. Азот входит в состав растительных белков. Животные получают готовые белковые вещества из растений; в животном организме содержится от 1 до 10% азота (по массе), в шерсти и в рогах — около 15%. Все важнейшие части клеток (цитоплазма, ядро, оболочка) построены из белковых молекул. Ещё большее значение имеют особые бактерии, живущие в клубеньках на корнях бобовых растений (клевера, гороха, вики, люпина и др.), которые называют клубеньковыми (рис. 126). Эти бактерии связывают свободный атмосферный азот, превращая его в соединения, которые усваивают растения, образуя белки своего организма. Соединения азота в почве пополняются также во время грозовых ливней. Как вы уже знаете, при этом из азота и кислорода образуется оксид азота (II), который под действием кислорода воздуха превращается в оксид азота (IV):
Последний взаимодействует с водой (также в присутствии кислорода воздуха), и получается азотная кислота:
Эта кислота, попадая в почву, реагирует с находящимися в ней соединениями натрия, кальция, калия и образует соли — селитры, необходимые для минерального питания растений (рис. 127).
Открытие азота. В 1772 г. английский учёный Д. Резерфорд и шведский исследователь К. Шееле в экспериментах по сжиганию веществ обнаружили газ, не поддерживающий дыхание и горение. Позднее, в 1787 г., А. Лавуазье установил наличие в воздухе газа, не поддерживающего дыхания и горения. По его предложению этому газу было дано название «азот», означающее «безжизненный» (от лат. а — нет и зоэ — жизнь). Другое латинское название — нитрогениум, введённое в 1790 г. Ж. Шапталем, означает «рождающий селитру».
1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания. 2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
1. Напишите уравнения реакций азота с магнием, кальцием, алюминием. Рассмотрите эти окислительно-восстановительные процессы. Как называют продукты реакций? Каков тип химической связи и кристаллической решётки в них? Какими свойствами должны обладать продукты реакций? 2. Напишите уравнения реакций, с помощью которых можно осуществить следующие переходы:
Рассмотрите первую реакцию как окислительно-восстановительную. 3. Дайте характеристику реакции по всем изученным вами признакам:
4. Определите, используя метод электронного баланса, коэффициенты в уравнениях реакций, соответствующих следующим схемам:
5. В лаборатории азот получают разложением нитрита аммония:
Придумайте и решите задачу, в условии которой была бы указана масса исходного вещества и массовая доля в нём примесей, а требовалось бы найти объём одного продукта и число молекул другого получаемого вещества.
|
|
|