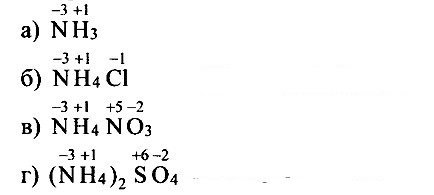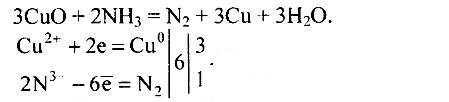|
|
|
|
|
Глава 3. Неметаллы Аммиак. ОтветыОтвет на вопрос 1Электронное строение молекулы аммиака: 3 испаренных электрона атома азота участвуют в формировании 3-х ковалентных связей с 3-мя атомами водорода. Общие электронные пары смещены в сторону более электроотрицательного атома азота. Пространственное строение: молекула аммиака имеет форму треугольной пирамиды. Ответ на вопрос 2Аммиак легко сжижается при обычном давлении и температуре -33,4°С, а при испарении жидкого газа из окружающей среды поглощается много тепла, поэтому он применяется в холодильных установках. Аммиак очень хорошо растворим в воде. 10 % раствор аммиака называется нашатырным спиртом и используется в медицине.Ответ на вопрос 3Водородная связь— это химическая связь между атомами водорода и атомами сильно электроотрицательных элементов (фтор, кислород, азот). Водородная связь образуется обычно между двумя соседними молекулами. Например, она образуется между молекулами воды, спиртов, фтороводорода, аммиака. Это очень слабая связь — примерно в 15-20 раз слабее ковалентной. Благодаря ей некоторые низкомолекулярные вещества образуют ассоциаты, что приводит к повышению температур плавления и кипения веществ. Аномально высокие температуры плавления и кипения характерны для воды (если рассматривать водородные соединения VI группы), Все водородные соединения VI группы, кроме воды, являются газами. Очень важную роль играет водородная связь в молекулах важнейших для живых существ соединений — белков и нуклеиновых кислот.Ответ на вопрос 4Водородные связи образуются между молекулами воды спиртов, кислой, галогенводородов, при этом аномально увеличиваются температуры плавления и кипения.Ответ на вопрос 5Катлон алюминия образуется в результате взаимодействия свободной (неподеленной / электронной пары атома азота молекулы аммиака с катионом водорода, переходящего к аммиаку от молекулы кислот или воды. Механизм образования ковалентной связи, которая возникает не в результате обобществления неспаренных электронов, а благодаря свободной электронной паре, имеющейся у одного из атомов, называют донорно-аклепторным. Т.е. Донорно-аклепторный — это не особый вид связи, а лишь особый механизм образования ковалентной связи.Ответ на вопрос 6При добавлении фенолфталеина к раствору аммиака, раствор окрасится в малиновый цвет, т.к. раствор аммиака имеет щелочную среду, так он, например, реагирует с кислотами: NH4OH + НСl → NH4Cl + H2O.Ответ на вопрос 7
Ответ на вопрос 8
Ответ на вопрос 9Аммиак проявляет только восстановительные свойства, т.к. азот находится в самой низкой степени окисления и не может больше принимать электроны.Ответ на вопрос 10
|
|
|