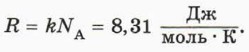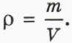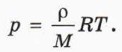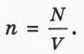|
|
|
|
|
§ 40. Уравнение состояния идеального газа Уравнение состояния идеального газа (уравнение Менделеева — Клапейрона)Вернемся теперь к соотношению
Произведение постоянной Больцмана k на постоянную Авогадро NA называют универсальной газовой постоянной и обозначают R:
Используя универсальную газовую постоянную, уравнение (6) можно переписать в виде
Это соотношение называют уравнением состояния идеального газа. Дело в том, что модель идеального газа (которую мы рассмотрим в следующем параграфе) хорошо описывает уже известные нам свойства всех достаточно разреженных газов, например окружающего нас воздуха. Уравнение идеального газа в виде формулы (7) предложил русский учёный Дмитрий Иванович Менделеев, поэтому его называют также уравнением Менделеева — Клапейрона.
Какие же задачи можно решать с помощью уравнения состояния идеального газа? Плотность газаНапомним, что плотность
Во многих задачах используют понятие нормальных условий для газа. По определению такими условиями называют давление 105 Па и температуру 0 °С = 273 К.
а) при нормальных условиях? б) при давлении 105 Па и комнатной температуре (20 °С)? Концентрация молекул газаКонцентрацией молекул n называют число молекул в единице объёма. Её можно выразить через число молекул N в данной массе газа и объём газа V:
Концентрация молекул измеряется в 1/м3. Зная концентрацию молекул и объём газа, можно найти число молекул в нём.
|
|
|



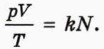
 14. Объясните, почему справедлива формула
14. Объясните, почему справедлива формула