|
|
|
|
|
§ 47. Применение первого закона термодинамики к газовым процессам Изопроцессы и адиабатный процесс (продолжение)
а) Чему равно конечное давление газа р2? б) Чему равен объём газа V? в) Начертите график этого же процесса в координатах (р, V). г) Чему равна работа газа Аг? д) Чему равно изменение внутренней энергии AU газа? е) Чему равно полученное газом количество теплоты Q?
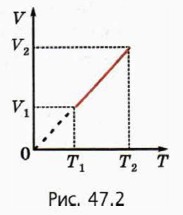
а) Чему равен конечный объём газа Т2? б) Чему равно давление газа р? в) Начертите график этого же процесса в координатах (р, V). г) Чему равна работа газа Аг? д) Чему равно изменение внутренней энергии газа? е) Чему равно полученное газом количество теплоты Q?
а) В каком случае количество теплоты больше? Во сколько раз больше? б) Объясните этот результат, используя закон сохранения энергии. Рассмотрим теперь изотермический и адиабатный процессы.
|
|
|



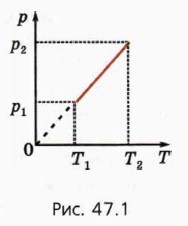
 4. На рисунке 47.1 изображён график зависимости р(Т) для v молей одноатомного идеального газа при изохорном переходе из состояния 1 в состояние 2. Даны начальные значения давления и температуры газа р1 и T1 конечная температура Т2.
4. На рисунке 47.1 изображён график зависимости р(Т) для v молей одноатомного идеального газа при изохорном переходе из состояния 1 в состояние 2. Даны начальные значения давления и температуры газа р1 и T1 конечная температура Т2.