|
|
|
|
Главная >> Молекулярная физика. Термодинамика. Физика 10 класс. Мякишев |
|
|
Глава 3. Температура. Газовые законы § 3.5. Газовые законы. Закон Бойля—Мариотта
Газовые законыИзменение одного из макроскопических параметров вещества определенной массы — давления р, объема V или температуры t — вызывает изменение остальных параметров. Если одновременно меняются все величины, характеризующие состояние газа, то на опыте трудно установить какие-либо определенные закономерности. Проще сначала изучить процессы, в которых масса и один из трех параметров — р, V или t — остаются неизменными. Количественные зависимости между двумя параметрами газа одной и той же массы при неизменном значении третьего параметра называют газовыми законами. Закон Бойля—МариоттаПервый газовый закон был открыт английским ученым Р. Бойлем (1627—1691) в 1660 г. Работа Бойля называлась «Новые эксперименты, касающиеся воздушной пружины». И действительно, газ ведет себя подобно сжатой пружине, в этом можно убедиться, сжимая воздух в обычном велосипедном насосе. Бойль изучал изменение давления газа в зависимости от объема при постоянной температуре. Процесс изменения состояния термодинамической системы при постоянной температуре называют изотермическим (от греческих слов isos — равный, thérme — тепло). Для поддержания температуры газа постоянной необходимо, чтобы он мог обмениваться теплотой с большой системой, в которой поддерживается постоянная температура, — термостатом. Термостатом может служить атмосферный воздух, если температура его заметно не меняется на протяжении опыта.
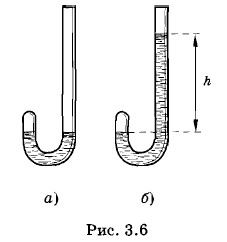
Бойль наблюдал за изменением объема воздуха, запертого в длинной изогнутой трубке столбом ртути (рис. 3.6, а). Вначале уровни ртути в обоих коленах трубки были одинаковыми и давление воздуха равно атмосферному (760 мм рт. ст.). Доливая ртуть в длинное колено трубки, Бойль заметил, что объем воздуха уменьшился вдвое, когда разность уровней в обоих коленах оказалась равной h = 760 мм, и, следовательно, давление воздуха увеличилось вдвое (рис. 3.6, б). Это навело Бойля на мысль о том, что объем данной массы газа и его давление находятся в обратно пропорциональной зависимости. Дальнейшие наблюдения за изменением объема при доливании различных порций ртути подтвердили это заключение. Независимо от Бойля несколько позднее французский ученый Э. Мариотт (1620—1684) пришел к тем же выводам. Поэтому найденный закон получил название закона Бойля—Мариотта. Согласно этому закону давление данной массы (или количества) газа при постоянной температуре обратно пропорционально объему газа: Если р1 — давление газа при объеме V1, p2 — его давление при объеме V2, то
Отсюда следует, что p1V1 = p2V2, или
Произведение давления газа данной массы на его объем постоянно, если температура не меняется. Этот закон справедлив для любых газов, а также для смесей газов (например, для воздуха). Убедиться в справедливости закона Бойля—Мариотта можно с помощью прибора, изображенного на рисунке 3.7. Герметичный гофрированный сосуд соединен с манометром, регистрирующим давление внутри сосуда. Вращением винта можно менять объем сосуда. Об объеме можно судить с помощью линейки. Меняя объем и измеряя давление, можно заметить, что уравнение (3.5.2) выполняется. Как и другие физические законы, закон Бойля—Мариотта является приближенным. При давлениях, в несколько сотен раз больших атмосферного, отклонения от этого закона становятся существенными. На графике зависимости давления от объема каждому состоянию газа соответствует одна точка.
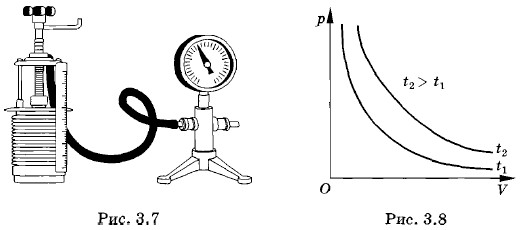
ИзотермыПроцесс изменения давления газа в зависимости от объема изображается графически с помощью кривой, которая носит название изотермы (рис. 3.8). Изотерма газа выражает обратно пропорциональную зависимость между давлением и объемом. Кривую такого рода называют гиперболой. Разным постоянным температурам соответствуют различные изотермы, так как более высокой температуре при одном и том же объеме соответствует большее давление*. Поэтому изотерма, соответствующая более высокой температуре t2, лежит выше изотермы, соответствующей более низкой температуре t1. * Подробнее об этом будет рассказано в дальнейшем. Молекулярно-кинетическое истолкование закона Бойля—МариоттаДавление газа зависит от числа ударов молекул о стенку сосуда. Число ударов прямо пропорционально числу молекул в единице объема (концентрации n). При уменьшении объема газа концентрация увеличивается, так как
|
|
|



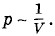


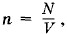 где N — число молекул в сосуде. Давление пропорционально концентрации и, следовательно, обратно пропорционально объему:
где N — число молекул в сосуде. Давление пропорционально концентрации и, следовательно, обратно пропорционально объему: 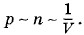 Так и должно быть согласно закону Бойля—Мариотта.
Так и должно быть согласно закону Бойля—Мариотта.