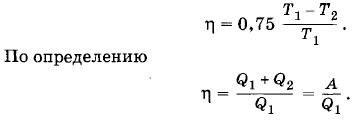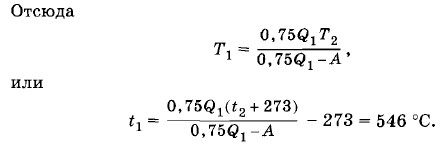|
|
|
|
Главная >> Молекулярная физика. Термодинамика. Физика 10 класс. Мякишев |
|
|
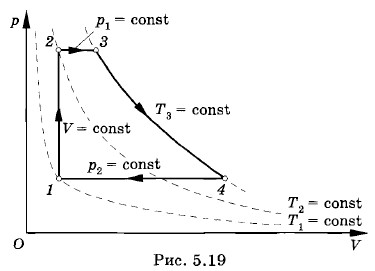
Глава 5. Законы термодинамики § 5.13. Примеры решения задач на тему: Законы термодинамикиЗадача 6В цилиндре под поршнем находится газ, состояние которого меняется следующим образом: при переходе из состояния 1 в состояние 2 давление увеличивается при постоянном объеме V; при переходе 2—3 увеличивается объем при постоянном давлении р1; переход 3—4 происходит с увеличением объема при постоянной температуре; при переходе 4—1 газ возвращается к первоначальному состоянию при постоянном давлении р2. Изобразите в координатах р, V; р, Т и V, Т графики изменения состояния газа и определите, при каких процессах газ получает теплоту, при каких отдает; как при этом меняется температура и какая работа совершается газом. Решение. График изменения состояния в координатах р, V приведен на рисунке 5.19. Процесс 1—2 — нагревание при постоянном объеме, температура увеличивается (Т2 > T1), следовательно, к газу подводится некоторое количество теплоты (Q > 0); работы газ не совершает (V = const, А'1 = 0).
Задача 7Одноатомный идеальный газ при давлении р1 = 3 • 105 Па и температуре t1 = 0 °С занимает объем V1 = 2 м3. Газ сжимают без теплообмена с окружающей средой, совершая при этом работу А = 35 кДж. Найдите конечную температуру газа Т2. Решение. Согласно формуле (15.8.1) для одноатомного идеального газа изменение внутренней энергии
ΔU = А. Следовательно, уравнение (5.13.17) можно записать так:
Задача 8Увеличится ли внутренняя энергия воздуха в комнате, если в ней протопить печь? Решение. Энергия единицы объема газа пропорциональна произведению абсолютной температуры газа на его плотность:U1 = сρТ, где с — постоянный коэффициент пропорциональности. Согласно уравнению состояния идеального газа
Задача 9Тепловая машина совершает работу А = 2 • 103 Дж при затрате количества теплоты Q1 = 4 • 103 Дж. Известно, что КПД такой машины составляет 0,75 (75%) максимально возможного КПД (ηmах)- Определите температуру нагревателя машины t1, если температура холодильника t2 = 0 °С. Решение. Согласно условию задачи КПД тепловой машины равен
<<< Примеры решения задач (к началу)
|
|
|



 Процесс 2—3 — изобарное расширение; температура увеличивается (Т3 > Т2); газ совершает положительную работу (A'2 > 0). Это видно из формулы А'2 = р1 (V3 — V2). Так как температура увеличивается, то внутренняя энергия тоже увеличивается, т. е. ΔU > 0. Поэтому из первого закона термодинамики в форме Q = ΔU + А'2 следует, что Q > 0, и при этом процессе к газу подводится некоторое количество теплоты.
Процесс 3—4 — изотермическое расширение; температура остается постоянной. Газ совершает положительную работу, так как он расширяется (А'3 > 0). Для изотермического процесса первый закон термодинамики имеет вид Q = А'3, поэтому Q > 0, т. е. теплота поглощается газом.
Процесс 2—3 — изобарное расширение; температура увеличивается (Т3 > Т2); газ совершает положительную работу (A'2 > 0). Это видно из формулы А'2 = р1 (V3 — V2). Так как температура увеличивается, то внутренняя энергия тоже увеличивается, т. е. ΔU > 0. Поэтому из первого закона термодинамики в форме Q = ΔU + А'2 следует, что Q > 0, и при этом процессе к газу подводится некоторое количество теплоты.
Процесс 3—4 — изотермическое расширение; температура остается постоянной. Газ совершает положительную работу, так как он расширяется (А'3 > 0). Для изотермического процесса первый закон термодинамики имеет вид Q = А'3, поэтому Q > 0, т. е. теплота поглощается газом.
 Процесс 4—1 — изобарное сжатие (V1 < V4); температура уменьшается (Т1 < Т4). Газ совершает отрицательную работу: А'4 = p2(V1 - V4). Так как газ охлаждается, то его внутренняя энергия уменьшается (ΔU < 0). Следовательно, как видно из первого закона термодинамики: Q = ΔU + А'4, газ отдает некоторое количество теплоты окружающим телам (Q < 0).
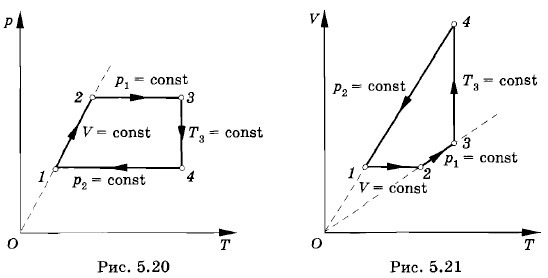
Графики изменения состояния в координатах р, Т и V, Т приведены на рисунках 5.20 и 5.21.
Процесс 4—1 — изобарное сжатие (V1 < V4); температура уменьшается (Т1 < Т4). Газ совершает отрицательную работу: А'4 = p2(V1 - V4). Так как газ охлаждается, то его внутренняя энергия уменьшается (ΔU < 0). Следовательно, как видно из первого закона термодинамики: Q = ΔU + А'4, газ отдает некоторое количество теплоты окружающим телам (Q < 0).
Графики изменения состояния в координатах р, Т и V, Т приведены на рисунках 5.20 и 5.21.
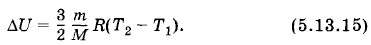 Из уравнения Менделеева—Клапейрона для начального состояния газа
Из уравнения Менделеева—Клапейрона для начального состояния газа 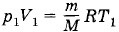 найдем
найдем
 Подставляя выражение (5.13.16) в уравнение (5.13.15), получим
Подставляя выражение (5.13.16) в уравнение (5.13.15), получим
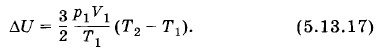 Так как газ сжимают без теплообмена с окружающей средой (адиабатный процесс), то в соответствии с первым законом термодинамики имеем
Так как газ сжимают без теплообмена с окружающей средой (адиабатный процесс), то в соответствии с первым законом термодинамики имеем
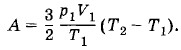 Откуда
Откуда
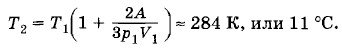
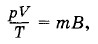 где В — постоянная величина.
Так как
где В — постоянная величина.
Так как 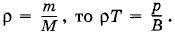 Следовательно,
Следовательно, 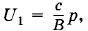 т. е. энергия определяется только давлением. Давление же в комнате равно атмосферному и не меняется при нагревании воздуха в комнате. Нагреваясь, воздух частично вытекает через щели наружу, что и обеспечивает постоянство энергии, несмотря на нагревание. Только в герметически закрытой комнате внутренняя энергия возрастала бы с нагреванием.
т. е. энергия определяется только давлением. Давление же в комнате равно атмосферному и не меняется при нагревании воздуха в комнате. Нагреваясь, воздух частично вытекает через щели наружу, что и обеспечивает постоянство энергии, несмотря на нагревание. Только в герметически закрытой комнате внутренняя энергия возрастала бы с нагреванием.