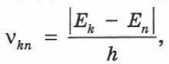|
|
|
|
|
§ 30. Атомные спектры Энергетические уровниОбъяснение линейчатых спектров в теории БораКак вы уже знаете из материала предыдущего параграфа, согласно постулатам Бора излучение и поглощение света атомом происходит только при переходе электрона с одной стационарной орбиты на другую. При этом частота излучённого или поглощённого света может принимать только определённый ряд значений:
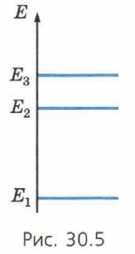
где Еk и Еn — уровни энергии, соответствующие стационарным состояниям. Так теория атома Бора объясняет линейчатый характер спектров излучения и поглощения атомов, а также то, что атомы каждого элемента излучают и поглощают свет с одними и теми же частотами, характерными только для этого элемента. Энергетические уровниЗначения энергии электрона в атоме называют энергетическими уровнями. При этом энергию электрона задают обычно в электрон-вольтах (сокращённо эВ). В предыдущем параграфе вы уже познакомились с этой единицей энергии. Напомним, что 1 эВ = 1,602 • 10-19 Дж. Схематическое изображение энергетических уровнейПри схематическом изображении энергетических уровней шкалу энергии обычно располагают вертикально, а сами уровни обозначают справа от этой шкалы горизонтальными отрезками. На рисунке 30.5 схематически изображены три энергетических уровня.
Если считать энергию свободного (удалённого от ядра на большое расстояние) покоящегося электрона равной нулю, то энергетические уровни связанных электронов (движущихся около ядра) должны соответствовать отрицательным значениям энергии. Объясним почему.
|
|
|