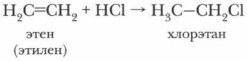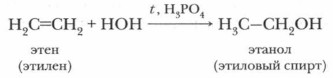|
|
|
|
|
Глава 5. Углеводороды § 15. Алкены. Свойства, применение и получение
Вы уже знакомы со свойствами этилена — первого представителя гомологического ряда алкенов. Теперь у вас есть возможность расширить и углубить свои знания об этом классе углеводородов. Физические свойства алкеновАлкены по физическим свойствам близки к алканам. Первые три члена гомологического ряда алкенов — газы: С2Н4, С3Н6, С4Н8. Углеводороды с числом атомов углерода от С5 до С18 — жидкости, остальные — твердые вещества. Как и алканы, они практически нерастворимы в воде. Хорошо растворяются в органических растворителях, таких как бензин, бензол, хлороформ и др. Они легче воды, с увеличением относительной молекулярной массы увеличиваются их температуры кипения и плавления. Химические свойства алкеновЭтиленовые углеводороды обладают большей химической активностью, чем предельные углеводороды. Проблема. От чего зависит химическая активность алкенов? Если мы рассмотрим пространственное строение алкенов, то увидим, что атомы углерода при двойной связи находятся в sр2-гибридизации и между ними образуется двойная связь, состоящая из π-связи и σ-связи (см. § 5). Пространственное расположение атомов в молекуле этилена показано с помощью моделей (рис. 27). Здесь π-связь менее прочная, чем σ-связь. При химической реакции π-связь у алкенов легко разрывается и к атомам углерода присоединяются другие атомы или группы атомов. Таким образом, для алкенов характерны реакции присоединения. Расширим свои знания о свойствах этиленовых углеводородов. 1. Реакции присоединенияа) Гидрирование (гидрогенизация) В присутствии катализатора (Ni, Pt) и при нагревании этиленовые углеводороды взаимодействуют с водородом с образованием предельных углеводородов (алканов):
Атомы углерода из состояния sр2-гибридизации переходят в состояние sр3-гибридизации. При этом изменяется и пространственное строение молекулы. Из плоской молекулы этилена образуется объемная молекула этана. б) Галогенирование Алкены вступают в реакцию с галогенами. Например, с хлором:
Дихлорэтан — бесцветная летучая жидкость со специфическим запахом, является хорошим растворителем. Токсические свойства дихлорэтана используются в сельском хозяйстве для борьбы с филлоксерой на виноградниках, а также для обеззараживания зернохранилищ.
При пропускании этилена и его гомологов через бромную воду происходит разрыв π-связи, атомы брома присоединяются к атомам углерода, окраска раствора исчезает. Эта реакция характерна для алкенов, она используется для распознавания этиленовых углеводородов. в) Гидрогалогенирование
Хлорэтан — бесцветный газ (при комнатной температуре), при небольшом охлаждении (до 12 °С) превращается в жидкость, испаряясь, поглощает большое количество теплоты. Это свойство используется в медицине при хирургических операциях, когда требуется местная анестезия. г) Гидратация
Эта реакция используется для получения этилового спирта в промышленности.
|
|
|



 Какие углеводороды называются непредельными, ненасыщенными? Объясните, почему они так называются.
Какие углеводороды называются непредельными, ненасыщенными? Объясните, почему они так называются.
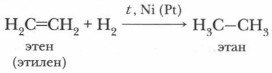
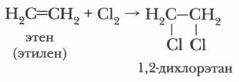
 Лабораторный опыт. Качественная реакция на этиленовые углеводороды. В пробирку с бромной водой пропустим этилен. Что вы наблюдаете? Запишите уравнение проведенной химической реакции. Дайте название полученному веществу.
Лабораторный опыт. Качественная реакция на этиленовые углеводороды. В пробирку с бромной водой пропустим этилен. Что вы наблюдаете? Запишите уравнение проведенной химической реакции. Дайте название полученному веществу.