|
|
|
|
|
Глава 5. Углеводороды § 17. Алкины. Свойства, применение и получение (окончание)2. Пиролиз метанаНачиная с 1970 г. более 50% ацетилена производится методом пиролиза из углеводородного сырья.
Равновесие химической реакции заметно смещается уже при температуре 1000-1300 °С и выше. При 1500 °С метан практически полностью превращается в ацетилен. Однако при этой температуре ацетилен начинает разлагаться на сажу и водород:
Таким образом, образование ацетилена происходит в промежуточной стадии разложения метана. Чтобы осуществить выход ацетилена, необходимо предотвратить его распад. Для этого необходимо уменьшить время пребывания углеводорода в зоне реакции, снижая давление и применяя «закалку» продуктов реакции путем быстрого охлаждения их до температуры, при которой не происходит реакция разложения. Основные понятия Реакции присоединения и замещения. Горение алкинов. Ацетилениды. Карбидный способ получения ацетилена. Пиролиз метана Вопросы и задания
а) метан и этан;
С2Н2 → С2Н4 → С2Н6 Как меняется строение молекул с изменением валентного состояния атома углерода?
Выводы 1. К непредельным углеводородам относятся алкены, алкадиены, алкины. 2. Алкены — непредельные углеводороды, в молекулах которых имеется одна двойная связь. Атомы углерода, соединенные двойной связью, находятся в состоянии sp2-гибридизации. Общая формула — СnН2n. В названии алкенов используется суффикс -ен. Для алкенов характерны: изомерия углеродной цепи, изомерия положения двойной связи, пространственная (геометрическая) изомерия и изомерия между классами. Алкены обладают большой химической активностью. За счет наличия π-связи алкены вступают в реакции присоединения и полимеризации. 3. Алкадиены — непредельные углеводороды, в молекулах которых имеются две двойные связи. Атомы углерода, связанные двойными связями, находятся в состоянии sр2-гибридизации. Общая формула алкадиенов — СnН2n-2. В названии используется суффикс -диен. Характерны изомерии: углеродной цепи, положения двойной связи, пространственная (геометрическая) и изомерия между классами. Характерные реакции — присоединения и полимеризации. При полимеризации диеновых углеводородов образуются каучуки, при вулканизации каучука — резина. 4. Алкины — непредельные углеводороды, в молекулах которых имеется одна тройная связь (одна σ-связь и две π-связи). Атомы углерода, связанные тройной связью, находятся в состоянии sp-гибридизации. Общая формула — СnН2n-2. В названии используется суффикс -ин. Характерны изомерии: углеродной цепи, тройной связи и изомерия между классами. Алкины вступают в реакции присоединения и замещения. 5. Для непредельных углеводородов качественной реакцией является обесцвечивание раствора перманганата калия и бромной воды.
|
|
|



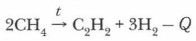
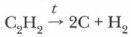
 1. С помощью раствора перманганата калия или бромной воды можно распознать:
1. С помощью раствора перманганата калия или бромной воды можно распознать:
 2. Какой объем хлороводорода понадобится для реакции с 10 л ацетилена (н. у.), чтобы получить винилхлорид?
2. Какой объем хлороводорода понадобится для реакции с 10 л ацетилена (н. у.), чтобы получить винилхлорид?
 3. Запишите уравнения реакций соответственно следующей схеме:
3. Запишите уравнения реакций соответственно следующей схеме: