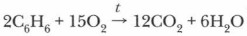|
|
|
|
|
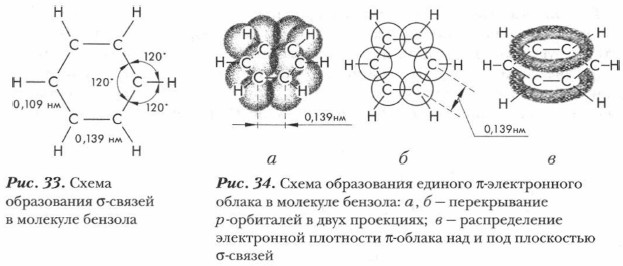
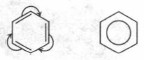
Глава 5. Углеводороды Ароматические углеводороды. БензолБолее точное представление о том, как в молекуле бензола размещены химические связи, можно получить, основываясь на современных представлениях об электронном строении молекулы бензола. Все атомы углерода в молекуле бензола находятся в sp2-гибридном состоянии. Каждый атом углерода образует три σ-связи: с двумя соседними атомами углерода и одним атомом водорода. Эти связи лежат в одной плоскости, и углы между ними равны 120° (рис. 33). Таким образом, шесть атомов углерода образуют правильный шестиугольник. Кроме того, каждый атом углерода имеет одну негибридную 2р-орбиталь, на которой находится один электрон. Негибридное р-электронная орбиталь каждого атома углерода перекрывается рядом находящимися негибридными π-электронными облаками слева и справа, образуется единое π-электронное облако, состоящее из шести электронов. Электронная плотность в нем распределена равномерно (рис. 34). Все связи между атомами углерода одинаковые. Перекрывание происходит над и под плоскостью σ-связей. С подобным явлением вы уже знакомились при изучении диеновых углеводородов, содержащих сопряженные двойные связи (см. § 16).
Исследования показали, что в бензоле нет простых и двойных связей, под влиянием π-электронного облака ядра атомов углерода сближаются, и расстояние между центрами соседних атомов углерода сокращается и становится одинаковым — 0,139 нм. Вспомним, что длина одинарной связи С—С равна 0,154 нм, а двойной связи С=С — 0,134 нм. В настоящее время используют следующие современные структурные формулы молекулы бензола:
Чаще всего пользуются формулой в виде правильного шестиугольника с окружностью в цикле. Электронное строение бензола объясняет загадки молекул бензола:
Плоскость, в которой расположены атомы углерода, называется бензольным ядром, или бензольным кольцом. Бензольное ядро — это прочная система. Связь в бензольном ядре часто называют ароматической. Делокализованная π-связь — главный признак принадлежности веществ к группе ароматических соединений. По международной номенклатуре ароматические углеводороды называются аренами.
Физические свойства бензолаБензол — это легкокипящая (температура кипения 80,1 °С) бесцветная жидкость, не растворяется в воде. Имеет специфический запах. При охлаждении легко застывает и превращается в белую кристаллическую массу с температурой плавления 5,5 °С. Химические свойства бензола1. Реакция горенияКак все углеводороды, бензол сгорает с образованием углекислого газа и воды:
Бензол горит коптящим пламенем. Задание. Вычислите массовую долю (%) углерода в бензоле.
|
|
|