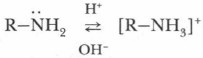|
|
|
|
|
Глава 10. Азотсодержащие соединения Строение и химические свойства аминов2. Будучи органическими основаниями, амины изменяют окраску индикаторов (лакмуса, фенолфталеина, метилоранжа) подобно растворам минеральных щелочей, так как в растворах аминов имеются анионы ОН-. Они образуются при взаимодействии аминов с водой. Например:
Образование новой N—Н связи осуществляется по донорно-акцепторному механизму, где атом азота — донор, предоставляющий свою неподеленную пару электронов в общее пользование, а протон (ион водорода) — акцептор, принимающий эту пару на свою свободную s-орбиталь. 3. Как основания амины взаимодействуют с минеральными кислотами. Например, при взаимодействии метиламина с соляной кислотой образуется соль — хлоридметиламин (его образование подобно образованию NH4Cl).
Подобным образом идет взаимодействие аминов и с другими кислотами (серной, уксусной, фосфорной и др.). Практически все амины реагируют с кислотами. В результате этой реакции образуются соли аминов. Хорошая растворимость солей аминов в воде, по сравнению с самими аминами, которые не все растворимы, учитывается в производстве лекарств: чаще используются соли, так как организм человека усваивает их легче, чем сами амины.
Задание. Вспомните качественную реакцию на соли аммония, запишите уравнение реакции. Амины из их солей можно выделить (как и аммиак из солей аммония), действуя на эти соли щелочами при слабом нагревании. Например: [CH3NH3]+Cl- + Na+OH- → CH3NH2↑ + Н2O + Na+Cl- или в общем виде:
Проблема. Как выяснить, какое из веществ: метиламин или аммиак — более сильное основание и почему? 4. Наличие углеводородного радикала усиливает осно́вные свойства аминов. СН3 → NH2
Проблема. Влияет ли характер углеводородного радикала на основность аминов? Приведите аргументы в пользу своих прогнозов. Обратите внимание не только на характер радикалов, но и на их число. Применение и получение алифатических аминовМетиламин и диметиламин — бесцветные газы. Триметиламин — вещество, имеющее «рыбный запах», является продуктом анаэробного дыхания морских организмов. Впервые его выделили в 1851 г. путем перегонки селедочного рассола с известковой водой. Амины широко распространены в природе. Их много в белковых пищевых продуктах. Например, триметиламин содержится в сельди. Он играет важную роль в биохимических процессах организма человека.
Амины широко используются в органическом синтезе как исходное сырье для получения красителей, пестицидов и других продуктов. Применяют амины и в фармацевтической промышленности для производства лекарственных средств, например аминазина, антигистаминных препаратов.
|
|
|



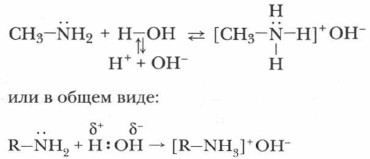
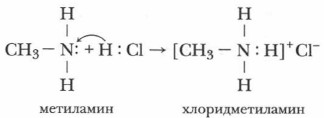
 Соли аминов являются ионными соединениями, поэтому имеют высокую температуру плавления, хорошо растворимы в воде.
Соли аминов являются ионными соединениями, поэтому имеют высокую температуру плавления, хорошо растворимы в воде.