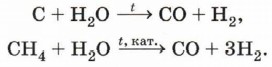|
|
|
|
|
Глава 3. Углеводороды § 10. АлканыНапомним, что углеводородами называются органические вещества, молекулы которых состоят из атомов двух химических элементов — углерода и водорода. Вы уже знаете, что все углеводороды можно разделить на две группы — предельные (насыщенные, не содержат кратных связей) и непредельные (ненасыщенные, содержат кратные связи). Важнейшим классом предельных углеводородов являются алканы.
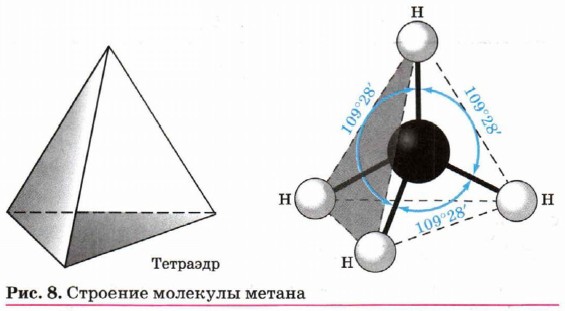
Строение алкановАлканы называют также парафиновыми углеводородами или парафинами (от лат. parum affinis — не обладающие сродством). Это название отражает низкую химическую активность алканов при комнатной температуре. Причина невысокой реакционной способности кроется в специфике строения молекул парафиновых углеводородов. В молекулах алканов орбитали всех атомов углерода находятся в состоянии sр3-гибридизации. Это означает, что все четыре гибридные орбитали атома углерода одинаковы по форме, энергии и направлены в вершины равносторонней треугольной пирамиды — тетраэдра. Углы между орбиталями равны 109°28' (рис. 8).
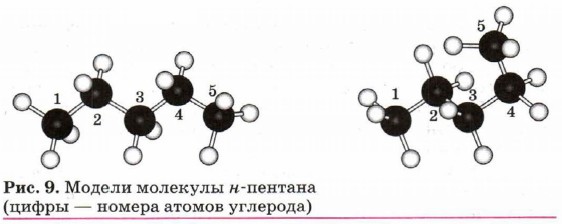
Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение, и молекулы алканов могут приобретать самую разнообразную форму. Молекулы имеют зигзагообразную форму с углами при атомах углерода, близкими к тетраэдрическому (109°28'), например в молекуле н-пентана (рис. 9). Все связи в молекулах алканов одинарные. Перекрывание происходит по линии, соединяющей ядра атомов, т. е. это σ-связи. Связи углерод—углерод являются неполярными и мало поляризуемыми. Длина С—С-связи в алканах равна 0,154 нм (1,54 • 10 - 10 м). Связи С—Н несколько короче. Электронная плотность лишь немного смещена в сторону более электроотрицательного атома углерода, т. е. связь С—Н является слабополярной.
Отсутствие в молекулах предельных углеводородов полярных связей приводит к тому, что они плохо растворяются в воде, не вступают во взаимодействие с заряженными частицами (ионами). Наиболее характерными для алканов являются реакции, протекающие с участием свободных радикалов.
Гомологический ряд метанаКак вы уже знаете, гомологи — это вещества, сходные по строению и свойствам и отличающиеся по составу на одну или более групп СН2. Предельные углеводороды составляют гомологический ряд метана. Названия и молекулярные формулы первых десяти гомологов приведены в таблице 3 (см. § 6). Изомерия и номенклатура алкановДля алканов характерна так называемая структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Как вам уже известно, простейший алкан, для которого характерны структурные изомеры, — это бутан.
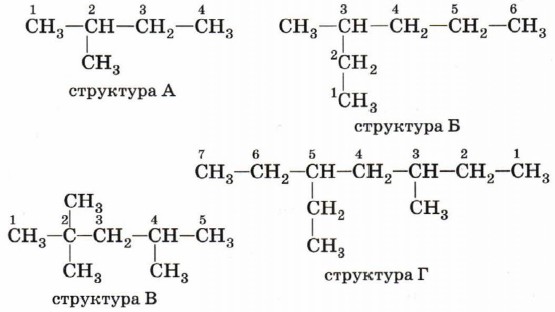
Основы номенклатуры ИЮПАК уже обсуждались. В этой части параграфа она будет более подробно рассмотрена для алканов. Формирование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле, которая является основой названия вещества. Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший заместитель (структура Г). Старшинство углеводородных заместителей определяется числом углеродных атомов. Падение старшинства, а также порядок перечисления заместителей в главной цепи соответствует ряду:
Обратите внимание, что название алкильных заместителей образуются от названия соответствующего алкана с заменой суффикса -ан на суффикс -ил. При формировании названия вначале указывают цифры — номера атомов углерода, при которых находятся заместители. Если при данном атоме находится несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую (2,2-). После номера через дефис указывают количество заместителей (ди — два, три — три, тетра — четыре, пента — пять) и название заместителя (метил, этил, пропил), затем без пробелов и дефисов — название главной цепи. Главная цепь называется как углеводород — член гомологического ряда метана, например пропан, бутан, пентан и т. д.).
Названия веществ, структурные формулы которых приведены выше, следующие: структура А: 2-метилбутан;
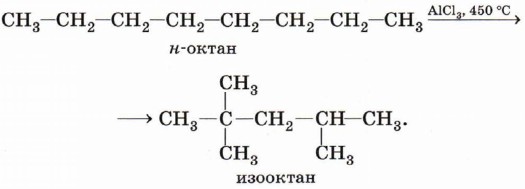
Получение алкановВыделение углеводородов из природного сырья. Источниками предельных углеводородов, как вы уже знаете, являются нефть и природный газ. Основной компонент природного газа — простейший углеводород метан, который используется непосредственно или подвергается переработке. Нефть, извлечённая из земных недр, также подвергается переработке: ректификации, крекингу. Природным источникам углеводородов посвящён §16 этого учебника. Алканы можно получать и синтетическими способами как в промышленности, так и в лабораторных условиях. Изомеризация. Линейные углеводороды при нагревании изомеризуются в углеводороды с разветвлённым скелетом. Изомеризация ускоряется при добавлении катализатора, например хлорида алюминия:
Гидрирование (присоединение водорода) алкенов. Как уже было сказано, в результате крекинга образуется большое количество непредельных углеводородов с двойной связью — алкенов. Уменьшить их количество можно, добавив в систему водород и катализаторы гидрирования — металлы (платина, палладий, никель):
Крекинг в присутствии катализаторов гидрирования с добавлением водорода называется восстановительным крекингом. Основными его продуктами являются предельные углеводороды. В заключение добавим, что повышение давления при крекинге (крекинг высокого давления) позволяет уменьшить количество газообразных Получение синтетического бензина. Смесь предельных углеводородов с числом углеродных атомов от 6 до 12 можно получить пропусканием смеси оксида углерода (II) и водорода над нагретым катализатором. Эту реакцию в 1926 г. впервые осуществили немецкие учёные Ф. Фишер и Г. Тропш:
Смесь оксида углерода (II) и водорода, получившую название «синтез-газ», довольно легко можно получить пропусканием перегретого водяного пара над углем (газификация угля) или конверсией природного газа водяным паром:
Мы рассмотрели несколько промышленных способов получения алканов, которые являются основой промышленной переработки основного углеводородного сырья — нефти и природного газа. Теперь обсудим несколько лабораторных способов получения алканов.
|
|
|




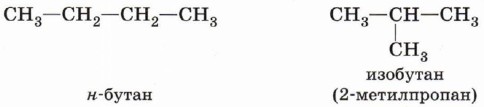
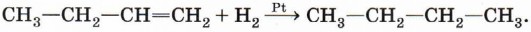
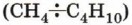 углеводородов и повысить содержание жидких углеводородов с длиной цепи 6—10 атомов углерода, которые составляют основу бензинов.
углеводородов и повысить содержание жидких углеводородов с длиной цепи 6—10 атомов углерода, которые составляют основу бензинов.