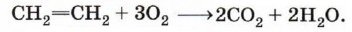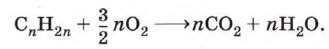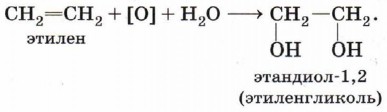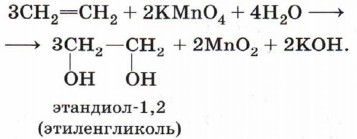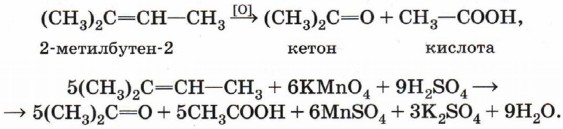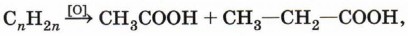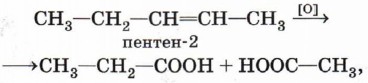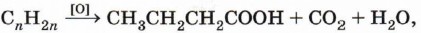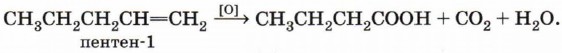|
|
|
|
|
Глава 3. Углеводороды § 11. Алкены (окончание)Все эти полимерные соединения находят широкое применение в самых разных областях человеческой деятельности (промышленности, медицине), используются для изготовления оборудования биохимических лабораторий, некоторые являются полупродуктами для синтеза других высокомолекулярных соединений (рис. 17).
Реакции окисления алкеновКак и любые органические соединения, алкены горят в кислороде с образованием СO2 и Н2O:
В общем виде:
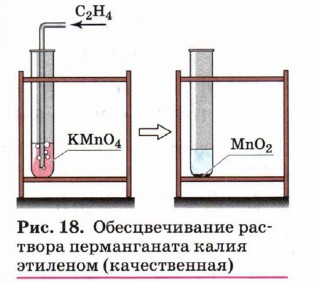
В отличие от алканов, которые устойчивы к окислению в растворах, алкены легко окисляются под действием водных растворов перманганата калия (рис. 18). В нейтральных или слабощелочных растворах на холоду происходит окисление алкенов до диолов (двухатомных спиртов), причём гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:
В действительности процесс окисления алкенов гораздо сложнее, происходящие при этом превращения можно отобразить уравнением:
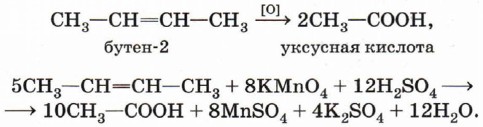
В кислой среде (подкисленный серной кислотой раствор) при нагревании происходит полное разрушение двойной связи и превращение атомов углерода, между которыми существовала двойная связь, в атомы углерода карбоксильной группы:
Если двойная связь находится у конца молекулы (например, в случае бутена-1), то одним из продуктов окисления должна оказаться муравьиная кислота — вещество, которое легко окисляется до углекислого газа и воды:
Если в молекуле алкена атом углерода при двойной связи содержит два углеводородных заместителя (например, 2-метилбутен-2), то при его окислении происходит образование кетона, так как превращение такого атома в атом карбоксильной группы невозможно без разрыва С—С-связи, относительно устойчивой в этих условиях:
Деструктивное окисление алкенов можно применять для определения их структуры. Так, например, если при окислении некоторого алкена получены уксусная и пропионовая кислоты:
это означает, что окислению подвергся пентен-2:
а если получены масляная (бутановая) кислота, углекислый газ и вода:
то исходный углеводород — пентен-1:
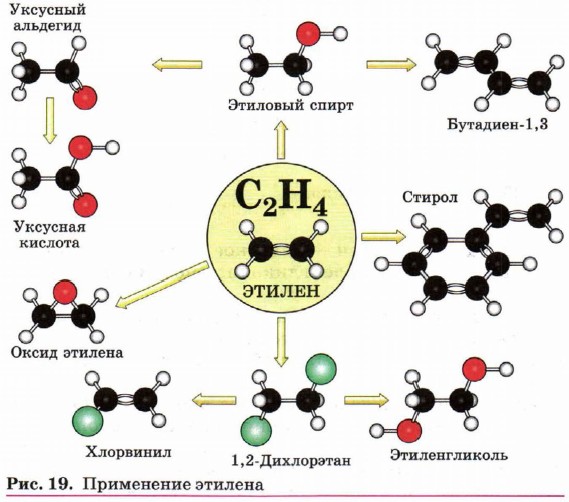
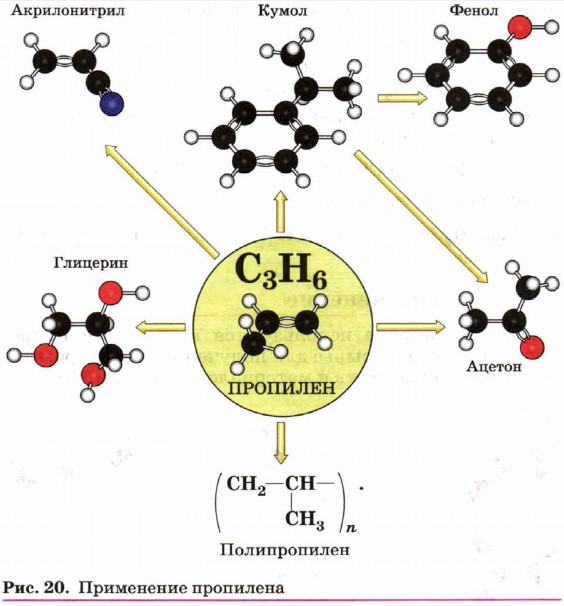
Применение алкеновАлкены широко используются в химической промышленности как сырьё для получения разнообразных органических веществ и материалов (рис. 19 и 20).
Так, например, этен — исходное вещество для производства этанола, этиленгликоля, эпоксидов, дихлорэтана. Большое количество этена перерабатывается в полиэтилен, который используется для изготовления упаковочной плёнки, посуды, труб, электроизоляционных материалов. Из пропена получают глицерин, ацетон, изопропиловый спирт, растворители. Полимеризацией пропена получают полипропилен, который по многим показателям превосходит полиэтилен: имеет более высокую температуру плавления, химическую устойчивость. В настоящее время из полимеров — аналогов полиэтилена производят волокна, обладающие уникальными свойствами. Так, например, волокно из полипропилена — одно из самых прочных синтетических волокон. Материалы, изготовленные из этих волокон, являются перспективными и находят всё большее применение в разных областях человеческой деятельности.
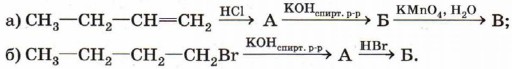
1. Какие виды изомерии характерны для алкенов? Напишите формулы возможных изомеров пентена-1. 2. Из каких соединений может быть получен: а) изобутен (2-метилпропен); б) бутен-2; в) бутен-1? Напишите уравнения соответствующих реакций. 3. Используя рисунок 20, перечислите области применения пропилена. 4. Расшифруйте следующую цепочку превращений. Назовите соединения А, Б, В:
5. Предложите способ получения 2-хлорпропана из 1-хлорпропана. Напишите уравнения соответствующих реакций. 6. Предложите способ очистки этана от примесей этилена. Напишите уравнения соответствующих реакций. 7. Приведите примеры реакций, с помощью которых можно различить предельные и непредельные углеводороды. 8. На полное гидрирование 2,8 г алкена израсходовано 0,896 л водорода (н. у.). Какова молекулярная масса и структурная формула этого соединения, имеющего нормальную цепь углеродных атомов?
9. Какой алкен находится в цилиндре, если известно, что на полное сгорание 20 см3 этого газа потребовалось 90 см3 (н. у.) кислорода?
10. При реакции алкена с хлором в темноте образуется 25,4 г дихлорида, а при реакции этого алкена той же массы с бромом в тетрахлорметане — 43,2 г дибромида. Установите все возможные структурные формулы исходного алкена. 11. Разделите лист бумаги пополам вертикальной чертой. Слева напишите 5 структурных формул алкенов, содержащих от 5 до 10 атомов углерода. Справа напишите названия этих углеводородов. Разрежьте лист по черте, передайте половинки двум одноклассникам, получите от них аналогичные половинки листков. Допишите по полученным формулам названия алкенов, по названиям — формулы. Проведите взаимопроверку. 12. Что такое сополимеры? При формулировании ответа на вопрос воспользуйтесь сайтом: http://www.xumuk.ru/encyklopedia/2/4145.html. Составьте уравнение реакции сополимеризации этилена и стирола.
|
|
|