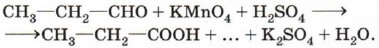|
|
|
|
|
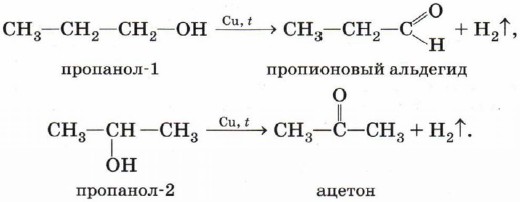
Глава 4. Кислородсодержащие соединения § 19. Альдегиды и кетоны (окончание)Способы получения альдегидов и кетоновАльдегиды и кетоны могут быть получены окислением или дегидрированием спиртов. Эти реакции подробно рассмотрены в § 17. Ещё раз отметим, что при окислении или дегидрировании первичных спиртов могут быть получены альдегиды, а вторичных спиртов — кетоны:
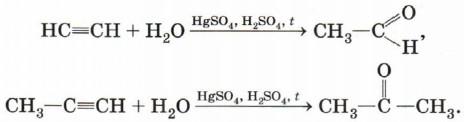
Реакция Кучерова (гидратация алкинов) рассмотрена в § 13. Напомним, что из ацетилена в результате реакции получается уксусный альдегид, из гомологов ацетилена — кетоны:
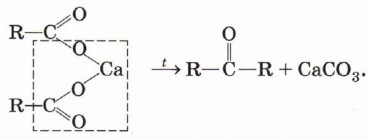
При нагревании кальциевых или бариевых солей карбоновых кислот образуется кетон и карбонат металла:
Отдельные представители альдегидов и их значениеФормальдегид (метаналь, муравьиный альдегид) НСНО — бесцветный газ с резким запахом и температурой кипения - 2 1 °С, хорошо растворим в воде. Ядовит! Раствор формальдегида в воде (40%) называют формалином и применяют для дезинфекции. В сельском хозяйстве формалин используют для протравливания семян, в кожевенной промышленности — для обработки кож. Формальдегид необходим для получения уротропина — лекарственного вещества. Иногда спрессованный в виде брикетов уротропин применяют в качестве горючего (сухой спирт). Большое количество формальдегида расходуется при получении фенолоформальдегидных смол и некоторых других веществ (см. рис. 44). Уксусный альдегид (этаналь) СН3СНО — жидкость с резким, неприятным запахом и температурой кипения 21 °С, хорошо растворим в воде. Ядовит! Из уксусного альдегида в промышленных масштабах получают уксусную кислоту и ряд других веществ, он используется для производства различных пластмасс.
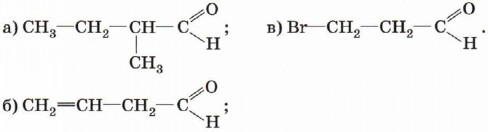
1. Сколько атомов углерода содержится в молекулах простейшего альдегида, простейшего кетона? Назовите эти вещества. Приведите синонимы их названий. 2. Назовите вещества, структурные формулы которых:
3. Составьте структурные формулы изомеров состава С4Н8O, содержащих карбонильную группу. К каким классам относятся эти вещества? Назовите их. Составьте уравнения реакций гидрирования этих соединений и укажите названия продуктов реакций. 4. Какой объём формальдегида (н. у.) необходимо подвергнуть гидрированию для получения 16 г метилового спирта?
5. Составьте уравнение реакции гидрирования диметилкетона (ацетона). Какова молярная масса продукта реакции? 6. В ходе реакции «серебряного зеркала» образовалась карбоновая кислота, имеющая относительную молекулярную массу, равную 88. Какие органические вещества могли быть реагентами в этой реакции? Используя структурные формулы, составьте возможные уравнения этой реакции. 7. Какая масса ацетальдегида необходима для восстановления 0,54 г серебра из его оксида? Какое количество вещества гидроксида калия необходимо для нейтрализации образующейся при этом уксусной кислоты?
8. В одном из сосудов находится раствор ацетона, в другом — ацетальдегида. Предложите способы определения содержимого каждого сосуда. 9. При сгорании 4,5 г органического вещества образовалось 3,36 л (н. у.) углекислого газа и 2,7 мл воды. Определите молекулярную и структурную формулы вещества, если его плотность по воздуху равна 1,035. Объясните этимологию названий этого вещества. Каковы области его применения? 10. Составьте уравнения реакций, протекающих при бромировании пропаналя на свету. Какие продукты образуются при этом? Назовите их. 11. При окислении гидроксидом меди (II) 11,6 г кислородсодержащего органического соединения образовалось 14,8 г одноосновной карбоновой кислоты, при взаимодействии которой с избытком гидрокарбоната натрия выделилось 4,48 л (н. у.) газа. Определите молекулярную и структурную формулы исходного соединения. 12. При окислении 1,18 г смеси муравьиного и уксусного альдегидов избытком аммиачного раствора оксида серебра образовалось 8,64 г осадка. Определите массовые доли альдегидов в смеси.
13. Выберите верные утверждения. Уксусный альдегид реагирует с: 1) гидроксидом меди (II);
Напишите уравнения возможных реакций. 14. Используя метод электронного баланса, составьте уравнение реакции:
Определите окислитель и восстановитель. 15. Выполните учебно-исследовательский проект на тему: «Ароматные молекулы: альдегиды и кетоны в природе и в жизни человека».
|
|
|