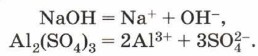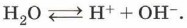|
|
|
|
|
Глава вторая. Химические реакции § 17. Роль воды в химических реакциях (продолжение)По величине степени диссоциации все электролиты можно условно разделить на сильные (степень диссоциации которых стремится к единице) и слабые (степень диссоциации которых стремится к нулю). Сильные электролиты в растворах практически полностью распадаются на ионы, и уравнение диссоциации для таких электролитов принято записывать как необратимый процесс:
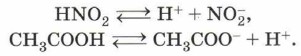
К сильным электролитам относят щёлочи, все соли, некоторые кислоты (НСl, HNO3, H2SO4, НСlO4, HBr, HI, CF3COOH и др.). Слабые электролиты в растворах диссоциируют очень незначительно, причём этот процесс обратим:
К слабым электролитам относятся многие неорганические (H2S, H2CO3, HCN) и почти все органические кислоты. Вода, будучи причиной диссоциации, сама незначительно диссоциирует:
Как молекулы, так и ионы в водных растворах гидратированы, т. е. связаны с окружающими их молекулами воды. Как вы знаете, автором одной из основополагающих теорий химии — теории электролитической диссоциации — является шведский химик С. Аррениус. Однако и русские химики — И. А. Каблуков и В. А. Кистяковский — внесли немалый вклад в развитие представлений о механизме диссоциации и поведении электролита в растворе.
Вспомните, что по характеру образующихся в результате диссоциации ионов различают три типа электролитов: кислоты, основания и соли.
Значительна роль воды для транспортировки веществ в сферу реакции. Как вы знаете, особенно важна она в жизни живых организмов, так как все жидкие среды (аммония или органического основания) более чем на 90—98% состоят из воды. Так, кровь разносит по организму кислород, питательные вещества, гормоны и другие биологически активные соединения и, в свою очередь, доставляет углекислый газ и продукты распада к местам их удаления из организма. О роли воды как транспортного средства в промышленном производстве мы уже достаточно рассказывали ранее. Не менее значима роль воды как участника химических реакций. В органической химии целая группа реакций присоединения носит название реакций гидратации. О реакции гидратации этилена мы говорили не раз, поэтому напомним о реакции гидратации ацетилена (реакции Кучерова), представляющей собой одну из ярких страниц отечественной органической химии.
|
|
|