|
|
|
|
|
Глава 6. Основные классы неорганических соединений Химические свойства кислот2. Кислота + оксид металла С этой группой реакций мы уже познакомились при изучении свойств основных оксидов: MgO + 2НСl = MgCl2 + Н2O
3. Кислота + растворимое основание (щёлочь)
К 2-3 мл раствора соляной кислоты добавьте 2-3 капли раствора лакмуса. Как изменилась окраска индикатора? Затем по каплям прилейте раствор гидроксида натрия и проследите за изменением окраски индикатора: от красной до фиолетовой и затем до синей. Дайте объяснения последовательному изменению окраски при постепенном приливании раствора щёлочи:
В кислой среде лакмус окрашивается в красный цвет. По мере прилива- ния щёлочи происходила нейтрализация кислой среды и возникала нейтральная (не кислая, не щелочная) среда, поэтому лакмус окрасился в фиолетовый цвет. Если щёлочи прилить столько, что её количество будет превышать количество кислоты, тогда эта избыточная, не прореагировавшая с кислотой щёлочь окрасит лакмус в синий цвет. Итак, в процессе обменного взаимодействия кислоты и щёлочи происходит нейтрализация среды, поэтому такие реакции называют реакциями нейтрализации. 2HNO3 + Са(ОН)2 = Ca(NO3)2 + 2Н2O
4. Кислота + нерастворимое основание
2Fe(OH)3↓ + 3H2SO4 = Fe2(SO4)3 + 6Н2O Итак, кислоты реагируют не только с растворимыми, но и с нерастворимыми основаниями. А в результате реакций образуются те же продукты — соль и вода. Таким образом, общее уравнение реакций для данного свойства совпадает с приведённым выше. Выводы 1. Кислоты вступают в химическое взаимодействие с металлами, их оксидами и гидроксидами — растворимыми и нерастворимыми. 2. Во всех случаях одним из продуктов взаимодействия оказывается соль. Основные понятия Генетический ряд •Реакции нейтрализации • Ряд активности металлов Вопросы и задания
а) Ва → ? → ? б) С → ? → ? в) Li → ? → ?
|
|
|



 К 2-3 мл раствора соляной кислоты добавьте 2-3 капли раствора лакмуса. Как изменилась окраска индикатора? Затем по каплям прилейте раствор гидроксида натрия и проследите за изменением окраски индикатора: от красной до фиолетовой и затем до синей. Дайте объяснения последовательному изменению окраски при постепенном приливании раствора щёлочи:
К 2-3 мл раствора соляной кислоты добавьте 2-3 капли раствора лакмуса. Как изменилась окраска индикатора? Затем по каплям прилейте раствор гидроксида натрия и проследите за изменением окраски индикатора: от красной до фиолетовой и затем до синей. Дайте объяснения последовательному изменению окраски при постепенном приливании раствора щёлочи:
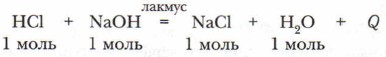
 1. Дополните схемы и составьте соответствующие им уравнения реакций:
1. Дополните схемы и составьте соответствующие им уравнения реакций:
 2. С какими из перечисленных веществ вступит в реакцию соляная кислота: SO2, CuO, HNO3, СO2, Fe(OH)3, КОН, Р2O5, СаО, Mg(OH)2? Составьте уравнения реакций.
2. С какими из перечисленных веществ вступит в реакцию соляная кислота: SO2, CuO, HNO3, СO2, Fe(OH)3, КОН, Р2O5, СаО, Mg(OH)2? Составьте уравнения реакций.