|
|
|
|
|
Глава 5. Подгруппа азота и ее типичные представители Азот как элемент и как простое вещество1. Взаимодействие азота с металлами. При повышенной температуре он соединяется со многими металлами, а при комнатной — только с литием, образуя нитриды соответствующих металлов, выступая в качестве их окислителя:
Большинство нитридов металлов — механически, термически и химически стойкие соединения, что позволяет использовать их в качестве высокопрочных материалов. 2. Взаимодействие азота с неметаллами. С неметаллами (S, Р, O2 и др.) азот взаимодействует при еще более высокой температуре. Так, реакция азота с кислородом начинается при температуре 3000-4000 °С (например, при электрическом разряде). Эта реакция эндотермическая (энергия связи в молекуле оксида азота (II) составляет 627 кДж/моль, т. е. значительно меньше, чем в молекуле азота):
Для азота известно много соединений и с атомами других элементов, но непосредственным взаимодействием простых веществ они, как правило, не получаются. Получение и применение азота. В промышленности азот получают из воздуха, используя различие в температурах кипения азота и кислорода. Азот широко применяют в химической промышленности для получения аммиака. В электротехнике и других отраслях промышленности он используется как инертная среда, например для заполнения электрических лампочек, при перекачке горючих жидкостей, сушке взрывчатых веществ и т. д. Применение азота предопределено его свойствами, в частности его химической инертностью. Основные понятия Физические свойства азота • Химические свойства азота • Применение азота Вопросы и задания
|
|
|



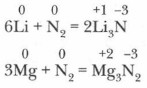
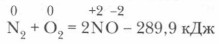
 Для осуществления реакций с участием азота требуется много энергии — он химически пассивен. Мы не всегда учитываем положительное значение этой химической пассивности. Не будь азот так инертен, в атмосфере он вступал бы в реакцию с кислородом воздуха, и жизнь на нашей планете перестала бы существовать, поскольку живые существа захлебнулись бы от несовместимых с жизнью оксидов азота, задохнулись бы в бескислородной атмосфере азота.
Для осуществления реакций с участием азота требуется много энергии — он химически пассивен. Мы не всегда учитываем положительное значение этой химической пассивности. Не будь азот так инертен, в атмосфере он вступал бы в реакцию с кислородом воздуха, и жизнь на нашей планете перестала бы существовать, поскольку живые существа захлебнулись бы от несовместимых с жизнью оксидов азота, задохнулись бы в бескислородной атмосфере азота.
 1. Рассчитайте относительную плотность молекулярного азота по воздуху.
1. Рассчитайте относительную плотность молекулярного азота по воздуху.
 2. Почему реакционная способность атома и молекулы азота различны?
2. Почему реакционная способность атома и молекулы азота различны?
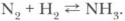
 7. В каком из следующих веществ: CO(NH2)2 (мочевина), NH4O3 (нитрат аммония) или NH4NO2 (нитрит аммония) — массовая доля азота максимальна?
7. В каком из следующих веществ: CO(NH2)2 (мочевина), NH4O3 (нитрат аммония) или NH4NO2 (нитрит аммония) — массовая доля азота максимальна?