|
|
|
|
|
Глава 6. Подгруппа углерода Оксиды углеродаФизические и химические свойства оксида углерода (IV)
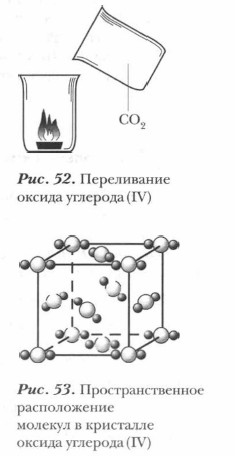
Оксид углерода (IV) СО2, или углекислый газ, — бесцветный газ, без запаха, малорастворимый в воде, в 1,5 раза тяжелее воздуха, поэтому его можно «переливать» из одного стакана в другой (рис. 52), не поддерживает горение и дыхание. При большой концентрации углекислого газа в воздухе человек и животные задыхаются. Часто он скапливается в опасных количествах в колодцах, шахтах, пещерах. Оксид углерода (IV) сжижается при комнатной температуре и высоком давлении. При испарении оксида углерода (IV) происходит его сильное охлаждение и он превращается в снегообразную массу — «сухой лед». У оксида углерода молекулярная кристаллическая решетка (рис. 53). Между молекулами действуют слабые межмолекулярные силы, поэтому при обычных условиях СО2, — газ. Оксид углерода (IV) — типичный кислотный оксид, следовательно, он: а) взаимодействует с основными оксидами с образованием солей: СO2 + СаО = СаСO3 б) растворяется в воде и частично с ней взаимодействует:
в) взаимодействует с основаниями: СO2 + Са(ОН)2 = СаСO3↓ + Н2O Эта реакция является качественной реакцией на углекислый газ. Оксид углерода (IV) нс поддерживает жизнедеятельность микроорганизмов, в том числе плесени, поэтому в его атмосфере хранят продукты. Применяется оксид углерода (IV) в производстве соды, сахара, для газирования воды и напитков, в жидком виде — в огнетушителях, в твердом виде («сухой лед») — для хранения продуктов, для получения искусственного льда в спорткомплексах. Основные понятия Угарный газ • Углекислый газ • Физические и химические свойства оксидов углерода • Качественная реакция на углекислый газ Вопросы и задания
|
|
|



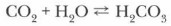
 1. Одна из пробирок наполнена азотом, а другая — углекислым газом. Как распознать эти газы?
1. Одна из пробирок наполнена азотом, а другая — углекислым газом. Как распознать эти газы?
 2. Рассмотрите с электронной точки зрения процесс образования молекулы оксида углерода (II) и ионов аммония и гидроксония. Что общего в этих процессах?
2. Рассмотрите с электронной точки зрения процесс образования молекулы оксида углерода (II) и ионов аммония и гидроксония. Что общего в этих процессах?
 8. На космическом корабле поглощение оксида углерода (IV) осуществляется сухим гидроксидом лития. Какой объем оксида углерода (IV) (н. у.) поглотится, если в результате реакции образуется 7,4 кг карбоната лития?
8. На космическом корабле поглощение оксида углерода (IV) осуществляется сухим гидроксидом лития. Какой объем оксида углерода (IV) (н. у.) поглотится, если в результате реакции образуется 7,4 кг карбоната лития?