|
|
|
|
|
Глава 9. Металлы главных и побочных подгрупп § 52. Распространение и роль металлов IIA-группы в природе. Жесткость воды
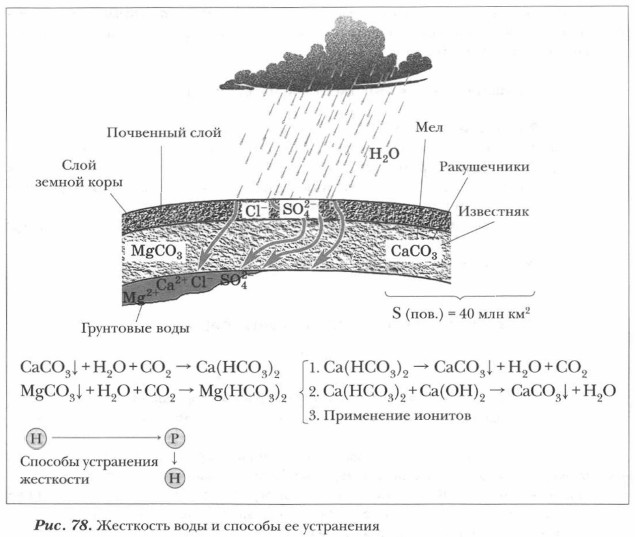
Металлы IIA-группы не встречаются в природе в свободном виде. Причина этого в их высокой химической активности. Зато геологическая роль их соединений исключительно велика. Вам известны такие горные породы, как мел, известняки, мрамор, — все они в основном образованы карбонатом кальция. В целом наиболее распространенными являются кальций и магний, а стронций и бериллий относятся к редким в природе элементам. Соединения кальция и магния в большом количестве содержатся в живых организмах и природных водах, как в морских, так и в пресных. В морской воде в среднем содержится 0,38% хлорида магния. Особый интерес представляет понятие о так называемой жесткости пресной воды. Жесткость воды обусловлена присутствием в ней солей кальция и магния. Как они попадают в воду? Рассмотрите рисунок 78.
Часть дождевых вод превращается в грунтовые воды. Они, в свою очередь, протекая в недрах Земли, соприкасаются с минералами кальция и магния, вымывая из них мелкие частички. В воде, насыщенной углекислотой (каковы источники С02, как происходит это насыщение?), нерастворимые карбонаты кальция и магния (средние соли) растворяются, так как превращаются в кислые соли (см. уравнения 1 и 2 на рис. 78). В таком растворимом виде гидрокарбонаты металлов остаются в воде и обусловливают ее временную жесткость. При кипячении воды гидрокарбонаты разлагаются и выпадают в осадок (вспомните накипь на стенках чайника). Нарастание таких осадков на стенках паровых котлов, труб неминуемо ведет к авариям. Это является серьезной причиной необходимости устранения жесткости воды. Помимо временной, существует еще так называемая постоянная жесткость, обусловленная присутствием в природной воде растворимых хлоридов и сульфатов кальция и магния. Основные понятия Жесткость воды: временная, постоянная Вопросы и задания
|
|
|



 Какие из элементов IIA-группы наиболее распространены в природе?
Какие из элементов IIA-группы наиболее распространены в природе?
 1. Какие свойства известняков способствуют их растворению в воде?
1. Какие свойства известняков способствуют их растворению в воде?
 2. Составьте формулы средних и кислых карбонатов, фосфатов и сульфатов кальция и магния. Что вы можете сказать об их распространении в природе и применении?
2. Составьте формулы средних и кислых карбонатов, фосфатов и сульфатов кальция и магния. Что вы можете сказать об их распространении в природе и применении?
 3. В чем сущность химических реакций, производимых с целью устранения временной жесткости воды? Напишите их уравнения и укажите условия протекания.
3. В чем сущность химических реакций, производимых с целью устранения временной жесткости воды? Напишите их уравнения и укажите условия протекания.