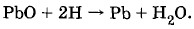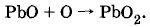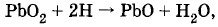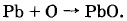|
|
|
|
|
Глава 2. Постоянный электрический ток § 2.13. Аккумуляторы
Принцип работы аккумулятораРабота аккумулятора основана на явлении поляризации электродов. Мы видели, что в гальванических элементах оно было вредным. Однако оказалось, что это явление можно использовать для практического получения электрического тока. Нальем в стакан раствор серной кислоты и опустим в него два одинаковых свинцовых электрода, поверхности которых покрыты оксидом свинца (II)
На электроде, соединенном с положительным полюсом источника тока (аноде), выделяется кислород, который окисляет оксид свинца (И) в оксид свинца (IV):
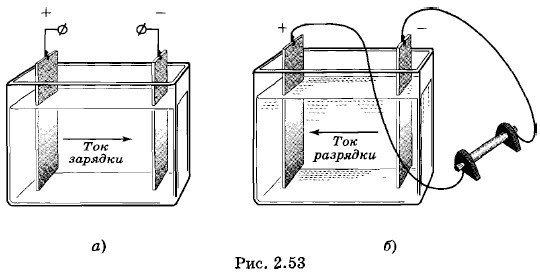
Таким образом, в результате пропускания тока через элемент, т. е. зарядки элемента, его электроды оказываются разными по химическому составу, и появляется определенная ЭДС — именно ЭДС поляризации, равная примерно 2 В. Элемент в таком состоянии уже сам является источником тока и при замыкании его на нагрузку может создавать в цепи в течение некоторого времени электрический ток (рис. 2.53, б) — ток разрядки, который направлен противоположно току зарядки. Такой элемент и есть аккумулятор. При разрядке химические реакции на электродах идут в обратном направлении. Положительная пластинка восстанавливается водородом:
а отрицательная пластинка окисляется кислородом:
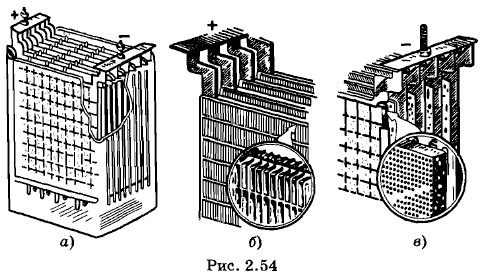
Как только обе пластинки окажутся одинаковыми, аккумулятор перестанет давать ток. Устройство кислотного (свинцового) аккумулятораРассмотренный нами аккумулятор не способен накопить сколько-нибудь значительный электрический заряд. Для увеличения его аккумулирующих способностей надо увеличить площадь поверхности электродов. Это достигается тем, что вместо электродов в виде пластин применяют блоки, заполненные активной массой. Положительные пластины, соединенные между собой свинцовой полосой, располагаются между отрицательными, также спаянными между собой (рис. 2.54, а). Эти блоки опускают в стеклянную банку с 20%-ным раствором серной кислоты. Положительные пластины (рис. 2.54, б) состоят из целого ряда скрепленных между собой параллельных вертикальных свинцовых ребер, образующих ячейки наподобие пчелиных сотов. В эти ячейки впрессовывается активная масса. У заряженного аккумулятора активная масса положительной пластины состоит из оксида свинца (IV) (РbO2). Положительные пластины имеют бурый цвет. Отрицательные пластины серого цвета (рис. 2.54, в) имеют остов в виде свинцовой решетки, ячейки которой тоже заполнены активной массой. В заряженном аккумуляторе активная масса отрицательных пластин — чистый свинец, имеющий пористую структуру и называемый поэтому губчатым свинцом. Расстояние между пластинами делается малым для уменьшения внутреннего сопротивления аккумулятора. Внутреннее сопротивление кислотных аккумуляторов очень мало, поэтому нельзя соединять клеммы аккумулятора проводником с малым сопротивлением (короткое замыкание), так как возникающий при этом сильный ток оказывает очень вредное действие на аккумулятор.
Для каждого аккумулятора существуют предельные значения силы тока при зарядке и разрядке. Эти данные указываются в паспорте аккумулятора. ЭДС кислотного аккумулятора сразу по окончании зарядки около 2,7 В. В начале работы аккумулятора она быстро падает до 2,1 В. Если ЭДС аккумулятора уменьшается до 1,8 В, его необходимо снова поставить на зарядку. Кроме кислотных аккумуляторов широкое распространение получили щелочные аккумуляторы. ЭДС щелочного аккумулятора равна примерно 1,3 В. Применение аккумуляторовВ современной электротехнике аккумуляторы находят широкое применение. Без них не могут работать автомобили. Аккумуляторы здесь нужны для запуска автомобильного двигателя при помощи стартера (специального электродвигателя), для освещения на остановках, когда генератор не работает. Аккумуляторы применяют для освещения железнодорожных вагонов на стоянках в поездах, курсирующих по дорогам, где нет пока электротяги. Аккумуляторы применяются на небольших электростанциях, например на электростанциях, использующих энергию ветра. Когда дует ветер и электрические генераторы работают на полную мощность, часть энергии идет на зарядку аккумуляторов. Затем энергию, запасенную в аккумуляторах, расходуют по мере надобности и независимо от метеорологических условий. Без аккумуляторов не могут обходиться подводные лодки (кроме атомных). Аккумуляторы применяют на электрокарах (электрических грузовых тележках), в электромобилях (автомобилях с электрическими двигателями), для питания радиоаппаратуры, рудничных ламп и во многих других случаях. Широко используются аккумуляторы в лабораторной практике, где они являются хорошими источниками постоянного тока.
|
|
|



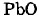 . Элемент в таком виде не обладает ЭДС, так как оба его электрода одинаковы. Присоединим теперь к электродам внешний источник тока (рис. 2.53, а) и пропустим через элемент ток (ток зарядки). Электрический ток, проходящий через водный раствор серной кислоты, вызовет разложение воды на водород и кислород. В результате на пластинке, соединенной с отрицательным полюсом источника тока (катоде), выделяется водород, который восстанавливает оксид свинца (II) в чистый свинец:
. Элемент в таком виде не обладает ЭДС, так как оба его электрода одинаковы. Присоединим теперь к электродам внешний источник тока (рис. 2.53, а) и пропустим через элемент ток (ток зарядки). Электрический ток, проходящий через водный раствор серной кислоты, вызовет разложение воды на водород и кислород. В результате на пластинке, соединенной с отрицательным полюсом источника тока (катоде), выделяется водород, который восстанавливает оксид свинца (II) в чистый свинец: