|
|
|
|
|
Глава 6. Свойства газов § 31. Газовые законы (окончание)Адиабатный процесс5. Вспомним опыт с сосудом, из которого при нагнетании в него воздуха вылетала пробка (см. рис. 71). В сосуде при этом образовывался туман, так как воздух, совершая работу, охлаждался и содержавшиеся в нём пары воды конденсировались. Процесс происходил настолько быстро, что теплообмен с окружающей средой не успевал осуществляться. Такой процесс называют адиабатным.
При адиабатном процессе системе не передаётся энергия, следовательно, Q = 0. В соответствии с первым законом термодинамики для адиабатного процесса можно записать: ΔU = —А., Из этого уравнения видно, что при расширении газ совершает работу, его внутренняя энергия уменьшается и температура понижается. Действительно, при расширении работа газа положительна (ΔV > 0), следовательно, А > 0, а изменение внутренней энергии отрицательно ΔU < 0. Подтверждением этого является опыт по адиабатному расширению воздуха. При быстром сжатии газа внешние силы совершают положительную работу, и внутренняя энергия газа увеличивается. Примером может служить опыт с воздушным огнивом (рис. 85). На дно толстостенного цилиндра кладут ватку, смоченную эфиром, резко ударяют по поршню, ватка воспламеняется. В этом случае при адиабатном сжатии воздуха и паров эфира их внутренняя энергия и, соответственно, температура возрастают.
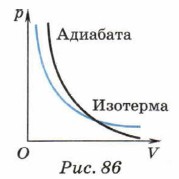
На рисунке 86 изображены графики зависимости давления от объёма при изотермическом и адиабатном процессах. Как видно, адиабата идёт круче, чем изотерма.
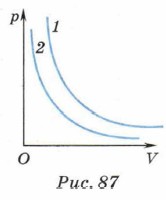
Вопросы для самопроверки 1. Что такое изопроцессы? 2. Как осуществить изотермический, изохорный, изобарный процессы? 3. Сформулируйте закон Бойля—Мариотта. Объясните его на основе молекулярно-кинетической теории. Запишите первый закон термодинамики для изотермического процесса. 4. Сформулируйте закон Гей-Люссака. Объясните его на основе молекулярно-кинетической теории. Запишите первый закон термодинамики для изобарного процесса. 5. Сформулируйте закон Шарля. Объясните его на основе молекулярно-кинетической теории. Запишите первый закон термодинамики для изохорного процесса. 6. Каковы границы применимости газовых законов? 7. Какой процесс называют адиабатным? Как его осуществить? Приведите пример адиабатного процесса. Упражнение 23 1. Закрытый сосуд, содержащий 5 л воздуха при давлении 1,6 • 105 Па, соединяют с сосудом ёмкостью 3 л, из которого откачан воздух. Какое давление установится в сосудах после их соединения, если считать, что температура воздуха остаётся неизменной? 2. Плотность водорода при нормальных условиях 9 • 10-2 кг/м3. Чему равна плотность водорода при увеличении давления до 3 • 105 Па при неизменной температуре? 3. На рисунке 87 приведены графики двух изотермических процессов. Какой из процессов происходит при более высокой температуре? Масса и химический состав газов, участвующих в процессах, одинаковы.
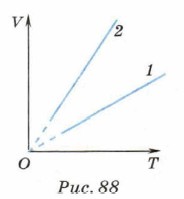
4. Какой объём займёт азот при температуре 200 °С, если при температуре 0 °С его объём равен 4 л? Считать, что изменение объёма происходит при постоянном давлении. 5. Горизонтально расположенный закрытый цилиндр разделён на две части подвижным поршнем. С одной стороны поршня в цилиндре содержится газ при температуре -73 °С, с другой стороны — тот же газ при температуре 27 °С. Поршень находится в равновесии. Определите объёмы, занимаемые газами, если общий объём цилиндра 500 см2. Массы газа, находящегося с обеих сторон от поршня, одинаковы. 6. Сравните давления, при которых происходят изобарные процессы, представленные графиками на рисунке 88.
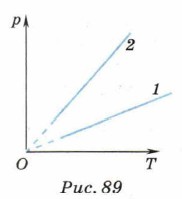
7. В цилиндре под поршнем находится воздух при давлении 2 • 105 Па и температуре 27 °С. Груз какой массы нужно положить на поршень после нагревания воздуха до температуры 50 °С, чтобы объём воздуха в цилиндре остался неизменным? Площадь поперечного сечения поршня 30 см2. 8. На рисунке 89 представлены графики двух изохорных процессов. Сравните объёмы газов, при которых они происходят, считая одинаковыми массу и химический состав газов.
Ответы 1. 105 Па. 2. 0,27 кг/м3. 3. Процесс 1. 4. ≈ 6,9 л. 5. 200 см3; 300 см3. 6. р1 > р2. 7. ≈ 64,6 кг. 8. V1 > V2.
|
|
|