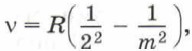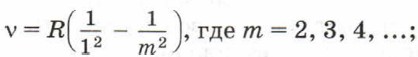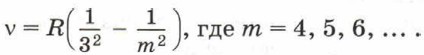|
|
|
|
|
Глава 7. Строение атома Испускание и поглощение света атомами. СпектрыЕщё один вид спектров — линейчатый. Линейчатый спектр испускания представляет собой чередование цветных линий различной яркости, разделённых широкими тёмными полосами. Линейчатый спектр испускания дают все вещества в газообразном атомарном состоянии. На рисунке V, б на форзаце представлен линейчатый спектр испускания атома водорода. Наличие цветных линий в спектре свидетельствует о том, что вещество излучает свет только вполне определённых частот. Спектр, в котором на цветной полосе сплошного спектра находятся тёмные линии, представляет собой линейчатый спектр поглощения. Получают линейчатый спектр поглощения, пропуская белый свет через холодный, неизлучающий газ. В подобном спектре, как и спектре испускания, появление полос означает, что поглощать (излучать) вещество может свет только определённых частот. Линии спектра поглощения располагаются точно в тех же местах спектра, в которых находятся линии спектра испускания для данного вещества. На рисунке V, в на форзаце представлен линейчатый спектр поглощения атома водорода. У каждого химического элемента свой линейчатый спектр испускания и поглощения, не совпадающий со спектром ни одного другого химического элемента. Спектральные закономерности3. Спектры изучались задолго до того, как стало известно строение атома. Впервые в 1885 г. швейцарскому учителю физики Я. Бальмеру в результате экспериментального исследования спектров атомарного водорода удалось получить формулу, по которой могли быть вычислены частоты четырёх линий в видимой части спектра водорода:
где R — некоторая постоянная величина, m = 3, 4, 5, ... . В настоящее время в видимой части спектра водорода обнаружено более 30 линий, частоты которых укладываются в формулу Бальмера. Эти линии в спектре водорода получили название серии Бальмера. Дальнейшие исследования спектра водорода показали, что в нём наблюдается ещё несколько серий спектральных линий. Так, в ультрафиолетовой области спектра была обнаружена серия спектральных линий (так называемая серия Лаймана), подчиняющаяся закономерности:
в инфракрасной части спектра водорода — серия Пашена
Всего в результате экспериментальных исследований учёными было обнаружено пять спектральных серий водорода. Используя законы классической механики и электродинамики, Бор смог определить значения энергии атома в различных стационарных состояниях и в результате пришёл к формулам, ранее полученным экспериментальным путём.
|
|
|