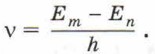|
|
|
|
|
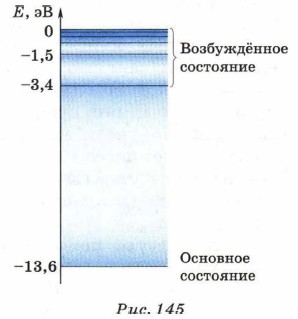
Глава 7. Строение атома § 44. Испускание и поглощение света атомами. СпектрыТеоретическое следствие теории Бора1. Постулаты Бора и построенная им теория атома водорода получили блестящее подтверждение в объяснении линейчатых спектров водорода. На рисунке 145 изображены дискретные значения энергии возможных стационарных состояний атома водорода. Все значения энергии — величины отрицательные. Это связано с тем, что энергию свободного покоящегося электрона принято считать равной нулю. Энергия же электрона внутри атома меньше энергии свободного электрона, поскольку для отрыва электрона от атома надо затратить работу по преодолению сил притяжения между отрицательно заряженным электроном и положительно заряженным ядром. Поэтому энергия связанного с атомом электрона меньше нуля. Энергия электрона в атоме водорода на первом энергетическом уровне минимальна и равна -13,6 эВ1. 1 В квантовой физике принято пользоваться единицей энергии электрон-вольт (эВ). 1 эВ = 1,6 • 10-19 Дж.
На этом уровне электрон может находиться бесконечно долго, поскольку это стационарное состояние невозбуждённого атома. Все остальные стационарные состояния атома с энергиями Е2, Е3 и т. д. являются возбуждёнными состояниями, из которых электрон может перейти на другой уровень в любой момент времени. Из второго постулата Бора можно определить частоту электромагнитного излучения атома водорода при переходе электрона из одного стационарного состояния с энергией Еm в стационарное состояние с энергией Еn:
Поскольку спектральные закономерности излучения атома водорода были уже известны, для подтверждения справедливости предложенных Бором постулатов необходимо установить их соответствие экспериментальным данным. Виды спектров2. Как вы уже знаете, при разложении солнечного света и света, излучаемого раскалёнными телами в твёрдом или жидком состоянии, можно наблюдать сплошной спектр. В сплошном спектре представлены все частоты электромагнитного излучения, и при наблюдении такого спектра можно видеть сплошную разноцветную полосу (рис. V, а на форзаце).
|
|
|