|
|
|
|
|
Глава 4. Строение атома и атомного ядра. Использование энергии атомных ядер § 52. Радиоактивность. Модели атомов
Предположение о том, что все тела состоят из мельчайших частиц, было высказано древнегреческими философами Левкиппом и Демокритом примерно 2500 лет назад. Частицы эти были названы атомами, что означает «неделимые». Атом — это мельчайшая, простейшая, не имеющая составных частей и поэтому неделимая частица. Но примерно с середины XIX в. стали появляться экспериментальные факты, которые ставили под сомнение представления о неделимости атомов. Результаты этих экспериментов наводили на мысль о том, что атомы имеют сложную структуру и что в их состав входят электрически заряженные частицы. Наиболее ярким свидетельством сложного строения атома явилось открытие явления радиоактивности, сделанное французским физиком Анри Беккерелем в 1896 г. Беккерель обнаружил, что химический элемент уран самопроизвольно (т. е. без внешних воздействий) излучает ранее неизвестные невидимые лучи, которые позже были названы радиоактивным излучением.
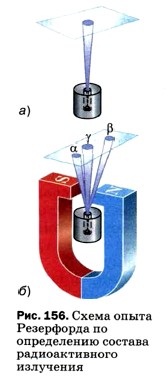
Поскольку радиоактивное излучение обладало необычными свойствами, многие учёные занялись его исследованием. Оказалось, что не только уран, но и некоторые другие химические элементы (например, радий) тоже самопроизвольно испускают радиоактивные лучи. Способность атомов некоторых химических элементов к самопроизвольному излучению стали называть радиоактивностью (от лат. radio — излучаю и activus — действенный). В 1899 г. в результате опыта, проведённого под руководством английского физика Эрнеста Резерфорда, было обнаружено, что радиоактивное излучение радия неоднородно, т. е. имеет сложный состав. Рассмотрим, как проводился этот опыт. На рисунке 156, (а) изображён толстостенный свинцовый сосуд с крупицей радия на дне. Пучок радиоактивного излучения радия выходит сквозь узкое отверстие и попадает на фотопластинку (излучение радия происходит во все стороны, но сквозь толстый слой свинца оно пройти не может). После проявления фотопластинки на ней обнаруживалось одно тёмное пятно — как раз в том месте, куда попадал пучок.
Потом опыт изменяли (рис. 156, б): создавали сильное магнитное поле, действовавшее на пучок. В этом случае на проявленной пластинке возникало три пятна: одно, центральное, было на том же месте, что и раньше, а два других — по разные стороны от центрального. Если два потока отклонились в магнитном поле от прежнего направления, значит, они представляют собой потоки заряженных частиц. Отклонение в разные стороны свидетельствовало о разных знаках электрических зарядов частиц. В одном потоке присутствовали только положительно заряженные частицы, в другом — отрицательно заряженные. А центральный поток представлял собой излучение, не имеющее электрического заряда. Положительно заряженные частицы назвали альфа-частицами, отрицательно заряженные — бета-частицами, а нейтральные — гамма-частицами или гамма-квантами. Некоторое время спустя в результате исследования различных физических характеристик и свойств этих частиц (электрического заряда, массы и др.) удалось установить, что β-частица представляет собой электрон, а α-частица — полностью ионизированный атом химического элемента гелия (т. е. атом гелия, потерявший оба электрона). Выяснилось также, что γ-излучение представляет собой один из видов, точнее диапазонов, электромагнитного излучения (см. рис. 136).
Явление радиоактивности, т. е. самопроизвольное излучение веществом α-, β- и γ-частиц, наряду с другими экспериментальными фактами, послужило основанием для предположения о том, что атомы вещества имеют сложный состав. Поскольку было известно, что атом в целом нейтрален, это явление позволило сделать предположение, что в состав атома входят отрицательно и положительно заряженные частицы. Опираясь на эти и некоторые другие факты, английский физик Джозеф Джон Томсон предложил в 1903 г. одну из первых моделей строения атома. По предположению Томсона, атом представляет собой шар, по всему объёму которого равномерно распределён положительный заряд. Внутри этого шара находятся электроны. Каждый электрон может совершать колебательные движения около своего положения равновесия. Положительный заряд шара равен по модулю суммарному отрицательному заряду электронов, поэтому электрический заряд атома в целом равен нулю. Модель строения атома, предложенная Томсоном, нуждалась в экспериментальной проверке. В частности, важно было проверить, действительно ли положительный заряд распределён по всему объёму атома с постоянной плотностью. Поэтому в 1911 г. Резерфорд совместно со своими сотрудниками провёл ряд опытов по исследованию состава и строения атомов.
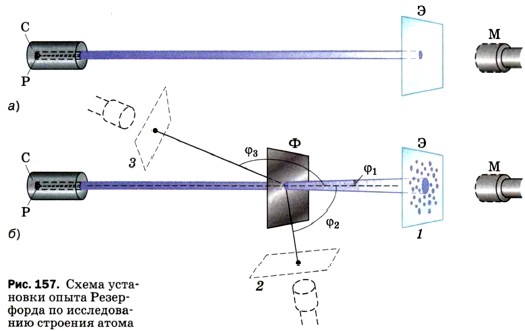
Чтобы понять, как проводились эти опыты, рассмотрим рисунок 157. В опытах использовался свинцовый сосуд С с радиоактивным веществом Р, излучающим α-частицы. Из этого сосуда α-частицы вылетают через узкий канал со скоростью порядка 15 000 км/с. Поскольку α-частицы непосредственно увидеть невозможно, то для их обнаружения служит стеклянный экран Э. Экран покрыт тонким слоем специального вещества, благодаря чему в местах попадания в экран α-частиц возникают вспышки, которые наблюдаются с помощью микроскопа М. Такой метод регистрации частиц называется методом сцинтилляций (т. е. вспышек). Вся эта установка помещается в сосуд, из которого откачан воздух (чтобы устранить рассеяние α-частиц за счёт их столкновений с молекулами воздуха). Если на пути α-частиц нет никаких препятствий, то они падают на экран узким, слегка расширяющимся пучком (рис. 157, а). При этом все возникающие на экране вспышки сливаются в одно небольшое световое пятно. Если же на пути α-частиц поместить тонкую фольгу Ф из исследуемого металла (рис. 157, б), то при взаимодействии с веществом α-частицы рассеиваются по всем направлениям на разные углы ср (на рисунке изображены только три угла: φ1, φ2 и φ3). Когда экран находится в положении 1, наибольшее количество вспышек расположено в центре экрана. Значит, основная часть всех а-частиц прошла сквозь фольгу, почти не изменив первоначального направления (рассеялась на малые углы). При удалении от центра экрана количество вспышек становится меньше. Следовательно, с увеличением угла рассеяния Ф количество рассеянных на эти углы частиц резко уменьшается. Перемещая экран вместе с микроскопом вокруг фольги, можно обнаружить, что некоторое (очень небольшое) число частиц рассеялось на углы, близкие к 90° (это положение экрана обозначено цифрой 2), а некоторые единичные частицы — на углы порядка 180°, т. е. в результате взаимодействия с фольгой были отброшены назад (положение 3). Именно эти случаи рассеяния α-частиц на большие углы дали Резерфорду наиболее важную информацию для понимания того, как устроены атомы веществ. Проанализировав результаты опытов, Резерфорд пришёл к выводу, что столь сильное отклонение α-частиц возможно только в том случае, если внутри атома имеется чрезвычайно сильное электрическое поле. Такое поле могло быть создано зарядом, сконцентрированным в очень малом объёме (по сравнению с объёмом атома).
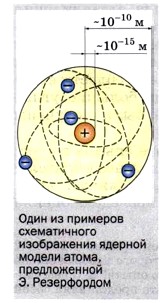
Поскольку масса электрона примерно в 8000 раз меньше массы α-частицы, электроны, входящие в состав атома, не могли существенным образом изменить направление движения α-частиц. Поэтому в данном случае речь может идти только о силах электрического отталкивания между α-частицами и положительно заряженной частью атома, масса которой значительно больше массы α-частицы. Эти соображения привели Резерфорда к созданию ядерной (планетарной) модели атома (о которой вы уже имеете представление из курса физики 8 класса). Напомним, что, согласно этой модели, в центре атома находится положительно заряженное ядро, занимающее очень малый объём атома. Вокруг ядра движутся электроны, масса которых значительно меньше массы ядра. Атом электрически нейтрален, поскольку заряд ядра равен модулю суммарного заряда электронов. Резерфорд сумел оценить размеры атомных ядер. Оказалось, что в зависимости от массы атома его ядро имеет диаметр порядка 10-14— 10-15 м, т. е. оно в десятки и даже сотни тысяч раз меньше атома (атом имеет диаметр около 10-10 м).
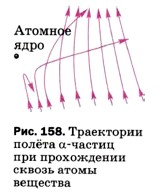
Рисунок 158 иллюстрирует процесс прохождения α-частиц сквозь атомы вещества с точки зрения ядерной модели. На этом рисунке показано, как меняется траектория полёта α-частиц в зависимости от того, на каком расстоянии от ядра они пролетают. Напряжённость создаваемого ядром электрического поля, а значит, и сила действия на α-частицу довольно быстро убывают с увеличением расстояния от ядра. Поэтому направление полёта частицы сильно меняется только в том случае, если она проходит очень близко к ядру. Поскольку диаметр ядра значительно меньше диаметра атома, то большая часть из числа всех α-частиц проходит сквозь атом на таких расстояниях от ядра, где сила отталкивания создаваемого им поля слишком мала, чтобы существенно изменить направление движения α-частиц. И только очень немногие частицы пролетают рядом с ядром, т. е. в области сильного поля, и отклоняются на большие углы. Именно такие результаты и были получены в опыте Резерфорда. Таким образом, в результате опытов по рассеянию α-частиц была доказана несостоятельность модели атома Томсона, выдвинута ядерная модель строения атома и проведена оценка диаметров атомных ядер. Вопросы1. В чём заключалось открытие, сделанное Беккерелем в 1896 г.?
|
|
|