|
|
|
|
|
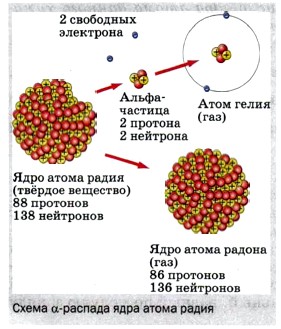
Глава 4. Строение атома и атомного ядра. Использование энергии атомных ядер § 53. Радиоактивные превращения атомных ядерВ 1903 г. (т. е. ещё до обнаружения существования атомных ядер) Резерфорд и его сотрудник, английский химик Фредерик Содди, обнаружили, что радиоактивный элемент радий в процессе α-распада (т. е. самопроизвольного излучения α-частиц) превращается в другой химический элемент — радон.
Дальнейшие опыты с различными радиоактивными препаратами показали, что не только при α-распаде, но и при β-распаде происходит превращение одного химического элемента в другой. После того как в 1911 г. Резерфордом была предложена ядерная модель атома, стало очевидным, что именно ядро претерпевает изменения при радиоактивных превращениях. Действительно, если бы изменения затрагивали только электронную оболочку атома (например, потеря одного или нескольких электронов), то при этом атом превращался бы в ион того же самого химического элемента, а вовсе не в атом другого элемента, с другими физическими и химическими свойствами. Реакция α-распада ядра атома радия с превращением его в ядро атома радона записывается так:
где знаком Число, стоящее перед буквенным обозначением ядра сверху, называется массовым числом, а снизу — зарядовым числом (или атомным номером). Массовое число ядра атома данного химического элемента с точностью до целых чисел равно числу атомных единиц массы, содержащихся в массе этого ядра. (Напомним, что одна атомная единица массы (сокращённо 1 а. е. м.) равна Зарядовое число ядра атома данного химического элемента равно числу элементарных электрических зарядов, содержащихся в заряде этого ядра. (Напомним, что элементарным электрическим зарядом называется наименьший электрический заряд, положительный или отрицательный, равный по модулю заряду электрона.) Можно сказать и так: зарядовое число равно заряду ядра, выраженному в элементарных электрических зарядах. Оба эти числа — массовое и зарядовое — всегда целые и положительные. Они не имеют размерности (т. е. единиц измерения), поскольку указывают, во сколько раз масса и заряд ядра больше единичных. По уравнению реакции можно увидеть, что ядро атома радия в результате излучения им α-частицы теряет приблизительно четыре атомные единицы массы и два элементарных заряда, превращаясь при этом в ядро атома радона. Эта запись является следствием того, что в процессе радиоактивного распада выполняются законы сохранения массового числа и заряда: массовое число (226) и заряд (88) распадающегося ядра атома радия равны соответственно сумме массовых чисел (222 + 4 = 226) и сумме зарядов (86 + 2 = 88) ядер атомов радона и гелия, образовавшихся в результате этого распада. Таким образом, из открытия, сделанного Резерфордом и Содди, следовало, что ядра атомов имеют сложный состав, т. е. состоят из каких-то частиц. Кроме того, стало ясно, что радиоактивность — это способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием частиц. Вопросы1. Что происходит с радиоактивными химическими элементами в результате α- и β-распада? Приведите примеры.
Упражнение 461. Определите массу (в а. е. м. с точностью до целых чисел) и заряд (в элементарных зарядах) ядер атомов следующих химических элементов: углерода 2. Сколько электронов содержится в атомах каждого из химических элементов, перечисленных в предыдущей задаче? 3. Определите (с точностью до целых чисел), во сколько раз масса ядра атома лития 4. Для ядра атома бериллия 5. Пользуясь законами сохранения массового числа и заряда, определите массовое число и заряд ядра химического элемента X, образующегося в результате следующей реакции β-распада:
где Найдите этот элемент в таблице Д. И. Менделеева на форзаце учебника. Как он называется?
|
|
|



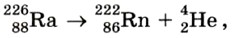
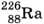 обозначено ядро атома радия, знаком
обозначено ядро атома радия, знаком 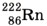 — ядро атома радона и знаком
— ядро атома радона и знаком 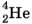 — α-частица, или, что то же самое, ядро атома гелия (т. е. ядра атомов обозначаются так же, как и сами атомы в таблице Д. И. Менделеева).
— α-частица, или, что то же самое, ядро атома гелия (т. е. ядра атомов обозначаются так же, как и сами атомы в таблице Д. И. Менделеева).
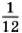 части массы атома углерода
части массы атома углерода 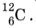 )
)
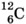 ; лития
; лития 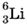 ; кальция
; кальция 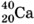 .
.
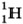 .
.
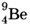 определите: а) массу ядра в а. е. м.
(с точностью до целых чисел); б) заряд ядра в элементарных электрических зарядах; в) число электронов в атоме.
определите: а) массу ядра в а. е. м.
(с точностью до целых чисел); б) заряд ядра в элементарных электрических зарядах; в) число электронов в атоме.
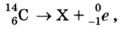
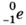 — β-частица (электрон).
— β-частица (электрон).