|
|
|
|
|
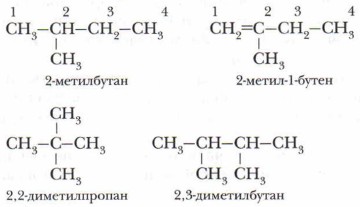
Глава 2. Теория строения органических соединений Теория химического строения А.М. БутлероваСтруктурные формулы часто используют в сокращённом варианте, что более удобно для обзора химического строения органических соединений. Например, эти же формулы изомеров пентана можно представить так:
Для соединений с длинными углеродными цепями существуют ещё более короткие варианты написания структурных формул. Например, пентан можно обозначить формулой СН3—(СН2)3—СН3. При изучении органических соединений, их разных классов, радикалов и других частиц используется номенклатура органических соединений. Теория химического строения послужила её упорядочению.
Номенклатура основывается на знании классов органических соединений (см. рис. 10, с. 36). В органической химии используются разные номенклатурные системы, однако общепризнанной является международная систематическая номенклатура IUРАС (ИЮПАК — Международный союз теоретической и прикладной химии). Номенклатура «этикетирует» элементы, вещества и частицы, помогает отличать их друг от друга. Вы будете постоянно использовать в единстве химические формулы и уравнения, номенклатуру и терминологию, дополняющие друг друга. В современной органической химии и в процессе её изучения для наименования соединений используется несколько номенклатур: историческая, рациональная и международная IUРАС. Историческая (тривиальная) номенклатура, возникшая ещё в древние времена, присваивала названия веществам преимущественно по их происхождению (муравьиная, яблочная, янтарная, щавелевая, винная кислоты, древесный спирт, мочевина и т. д.). Исторические названия наиболее распространенных в быту веществ используются и в наше время. По мере развития химии историческую номенклатуру сменила рациональная. Рациональную номенклатуру целесообразно применять для простейших углеводородов с разветвлённой цепью. Например, все предельные углеводороды рассматривают как производные метана, где один или все четыре атома водорода замещены на одновалентный радикал. При этом атом углерода, связанный с одним атомом углерода, называется первичным (—СН3), с двумя — с двумя — вторичным (—СН2—), с тремя — третичным Например:
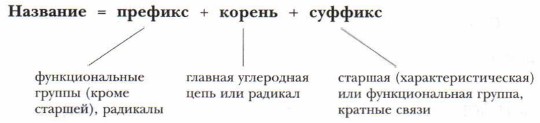
Рациональная номенклатура позволяет сравнительно легко называть простые вещества, и мы будем использовать её при изучении таких соединений, но она весьма затрудняет составление названий сложных веществ и разных изомеров. Поэтому ведущей в современной органической химии является международная номенклатура IUРАС. В основу международной номенклатуры IUPAC положены названия предельных углеводородов. Класс соединений согласно этой номенклатуре обозначается функциональным окончанием или суффиксом. Для обозначения предельных углеводородов используется суффикс -ан (пропан C3H8), для этиленовых -ен (пропен С3Н6), для ацетиленовых -ин (пропин С3Н4), для спиртов -ол (пропанол С3Н5—ОН), для альдегидов -аль (пропаналь С2Н5—СНО), для кислот -овая (пропановая кислота С2Н5СООН). С номенклатурой разных классов соединений вы уже знакомились в курсе химии 9 класса и продолжите её изучение в курсе органической химии в 10 классе. Далее мы покажем принципы составления названий и формул органических соединений на более простых, знакомых вам соединениях, преимущественно на углеводородах и их изомерах. Правила составления названий органических соединений1. Выбирается главная цепь — самая длинная непрерывная углеродная цепь, которая содержит функциональную группу или характерную для углеводородов двойную либо тройную связь. 2. Нумерация углеродных атомов главной цепи начинается с того конца, к которому ближе заместитель или функциональная группа. 3. Положение углеводородного радикала (начиная с простейшего) определяется атомом углерода главной цепи, с которым он связан. 4. Называется предельный углеводород, соответствующий главной цепи, и изменяется или прибавляется суффикс, соответствующий данному классу соединений. 5. Углеводородные остатки или радикалы, находящиеся в боковой цепи, рассматриваются как заместители водородных атомов в главной цепи. Заместителями могут быть галогены и некоторые функциональные группы, например аминогруппа —NH2, нитрогруппа — NO2 и др.
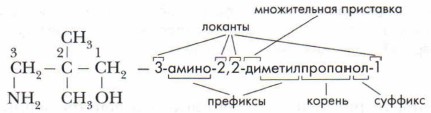
Корень — его название зависит от количества атомов углерода в цепи: С1 — «мет»; С2 — «эт»; С3 — «проп»; С4 — «бут»; С5 — «пент»; С6 — «гекс»; С7 — «гепт»; С8 — «окт»; С9 — «нон»; С10 — «дек». Суффикс указывает на определённый вид связи атомов углерода в соединении: —С—С— (алканы) -ан; Префикс используется в названиях более сложных соединений для обозначения каких-либо атомов или групп, входящих в их состав. Кроме префикса, корня и суффикса для составления названий сложных соединений используют локанты и множительные приставки. Локанты — цифры или буквы, которые указывают положение заместителей и кратных связей, они могут ставиться перед префиксом или после суффикса. Множительные приставки указывают число одинаковых заместителей или кратных связей: два — «ди-»; три — «три-»; четыре — «тетра-»; пять — «пента-»; шесть — «гекса-»; семь — «гепта-»; восемь — «окта-»; девять — «нано-». Например:
Примеры составления названий углеводородов, известных вам из 9 класса:
Для раскрытия содержания той или иной теории и реализации её функций важно придерживаться определённого плана, или алгоритма, её описания. План-характеристика теории1. Предпосылки создания теории (исторический аспект).
Теория химического строения обеспечила бурный расцвет синтеза органических веществ и химической промышленности. Как фундаментальная теория она нашла своё дальнейшее развитие на основе новых данных о строении и свойствах органических веществ и современных методов их исследования. Выводы 1. Стержнем теории А.М. Бутлерова является поня тие «химическое строение», под которым понимается последовательность соединения атомов в соответствии с их валентностью, их взаимное влияние друг на друга. 2. Основная идея теории — зависимость свойств органических веществ от их химического строения (что в равной степени относится и к неорганическим соединениям). Сущность теории раскрывают её основные положения. 3. Химическое строение органических соединений кратко и однозначно отражают структурные формулы и дополняющая их номенклатура. Каждое вещество имеет только одну структурную формулу. 4. Важнейшей функцией теории является объяснение явлений. Теории также присущи функции обобщения, прогнозирования и систематизации. 5. Каждое вещество любого класса имеет своё название. Для наименования органических соединений применяют разные номенклатуры: тривиальную (историческую), рациональную и международную систематическую (IUPAG). 6. Для написания названий и формул соединений следует знать правила их составления. Основные понятия Теория химического строения • Химическое строение • Структурная изомерия • Структурная формула • Номенклатура органических соединений Вопросы и задания
|
|
|



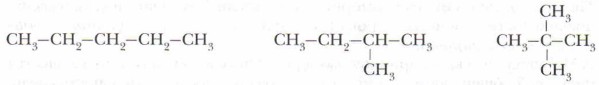
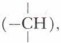 с четырьмя — четвертичным
с четырьмя — четвертичным 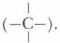
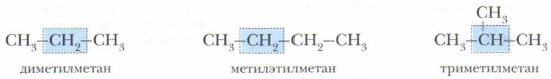
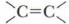 (алкены) -ен;
(алкены) -ен; 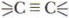 (алкины) -ин.
(алкины) -ин.
 Теория химического строения А.М. Бутлерова прочно вошла в науку и приобрела большое научное и практическое значение. Она стала важнейшей частью теоретического фундамента органической химии, руководящей основой всех её исследований. По своей значимости теория химического строения сопоставима с периодической системой химических элементов Д.И. Менделеева. Подобное признание вклада А.М. Бутлерова в науку и оценку его теории сделал дважды лауреат Нобелевской премии, крупнейший химик XX в. Л. Полинг: «Среди великих химиков мира я хотел бы назвать также Бутлерова (наряду с Менделеевым), установившего, что каждое вещество состоит из молекул, имеющих различную структуру, которая определяет качество вещества» (1975).
Теория химического строения А.М. Бутлерова прочно вошла в науку и приобрела большое научное и практическое значение. Она стала важнейшей частью теоретического фундамента органической химии, руководящей основой всех её исследований. По своей значимости теория химического строения сопоставима с периодической системой химических элементов Д.И. Менделеева. Подобное признание вклада А.М. Бутлерова в науку и оценку его теории сделал дважды лауреат Нобелевской премии, крупнейший химик XX в. Л. Полинг: «Среди великих химиков мира я хотел бы назвать также Бутлерова (наряду с Менделеевым), установившего, что каждое вещество состоит из молекул, имеющих различную структуру, которая определяет качество вещества» (1975).
 1. Раскройте основные исторические этапы создания теории химического строения.
1. Раскройте основные исторические этапы создания теории химического строения.
 3. Составьте структурные формулы: а) углеводорода пентана С5Н12; б) сероводорода; в) оксида углерода (IV). Какую информацию о химическом соединении они несут?
3. Составьте структурные формулы: а) углеводорода пентана С5Н12; б) сероводорода; в) оксида углерода (IV). Какую информацию о химическом соединении они несут?
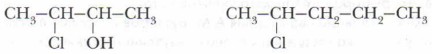
 5. Какое значение имела теория химического строения для науки и практики? Используя дополнительную литературу и другие источники информации, составьте тезисы кратких сообщений по этому вопросу (по выбору).
5. Какое значение имела теория химического строения для науки и практики? Используя дополнительную литературу и другие источники информации, составьте тезисы кратких сообщений по этому вопросу (по выбору).