|
|
|
|
|
Глава 2. Теория строения органических соединений § 2. Теория химического строения А.М. БутлероваТеория (от греч. theoria — «исследование») — это система обобщённых знаний, объясняющих те или иные стороны действительности. Ядро любой теории составляют её основные понятия и законы, а суть теории выражают её основные положения. Теория является важным инструментом научного познания, направлена на обобщение, систематизацию, объяснение и предсказание явлений. Изученная и усвоенная теория становится средством добывания новых знаний.
К концу 50-х гг. XIX в. органическая химия накопила массу фактов об органических веществах и их свойствах. Методом экспериментального анализа были определены качественный и количественный состав многих природных органических соединений и их молекулярные формулы. Но этот материал не был достаточно систематизирован. Ряд особенностей органических соединений (они рассмотрены в § 1) не находили объяснения на основе имеющихся в то время теоретических представлений, например явление изомерии, открытое ещё в 20-е гг. XIX столетия. Учёных смущало и то, что многие органические соединения имели несколько химических формул. Например, хорошо известной уксусной кислоте приписывали два десятка формул. В науке насущными стали вопросы: являются ли молекулы органических веществ беспорядочным нагромождением атомов, или же они имеют упорядоченное строение, и можно ли его установить путём экспериментального исследования веществ? Убеждённым сторонником познаваемости строения органических веществ был А.М. Бутлеров.
К 50-м гг. XIX в. острой стала задача выявления зависимости свойств веществ не только от состава, но и от их строения. Требовалась теория, способная обобщить и систематизировать накопленный материал, объяснить строение органических веществ. Её отсутствие заметно тормозило развитие науки. Такую теорию в 60-е гг. создал известный русский химик Александр Михайлович Бутлеров, назвавший её теорией химического строения. Основную идею и положения своей теории А.М. Бутлеров сформулировал в 1861 г. в статье «О химическом строении вещества». Под химическим строением он понимал последовательность соединения атомов в молекулах. При создании теории учёный опирался на известные к тому времени представления о четырёхвалентности атома углерода, способности его атомов соединяться между собой, образуя углеродные цепи, а также на уже разграниченные понятия «атом» и «молекула». А.М. Бутлеров отмечал, что чёткие представления о химической частице и определение понятий «атом» и «молекула» были самым существенным успехом химии, позволившим перейти к выявлению химического строения веществ.
В основу теории химического строения были положены фундаментальные понятия: «химические частицы (атомы, молекулы)», «валентность», «химическое строение», «изомерия». Основные положения теории химического строения1. Атомы в молекулах соединены в определённой последовательности химическими связями. Порядок связи атомов называется химическим строением. Изменение этой последовательности приводит к образованию нового вещества с новыми свойствами. 2. Соединение атомов в молекулу происходит в соответствии с их валентностью. Валентность углерода в органических веществах равна IV. 3. Свойства веществ зависят не только от их качественного и количественного состава, но и от того, в каком порядке атомы в молекуле соединены, т. е. от химического строения их молекул. 4. Многие органические вещества способны к изомерии. 5. Порядок связи атомов (химическое строение молекул) можно изучать и устанавливать химическими методами. 6. Атомы или группы атомов в молекуле взаимно влияют друг на друга, что сказывается на реакционной способности молекулы. Наиболее сильно влияют друг на друга атомы, непосредственно связанные между собой. Это положение в равной степени относится как к органическим, так и к неорганическим веществам. Следствия теории химического строенияИзомерия — важнейший объект, явленние и понятие теории химического строения.
Важным положением теории А.М. Бутлерова является объяснение способности многих органических веществ к изомерии, установление причины этого явления. Утверждению этого положения теории способствовало предсказание Бутлеровым существования двух изомеров бутана с общей формулой С4Н10: СН3—СН2—СН2—СН3 (нормальный бутан) и Предсказание и синтез изомеров бутана стали блестящим подтверждением правильности теории Бутлерова и выявили её основные функции — объяснение и прогнозирование. А.М. Бутлеров вскрыл причину изомерии. Она состоит в том, что вещества с одинаковой общей формулой могут иметь разную последовательность соединения атомов в молекуле, то есть различаться химическим строением. Позднее такие соединения были названы структурными изомерами.
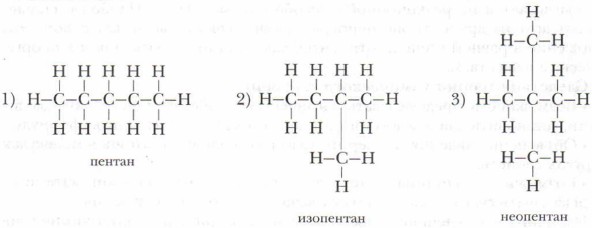
Каждой теории химии присущ свой научный язык (символика, номенклатура, терминология). Для изображения структурных изомеров А.М. Бутлеров использовал структурные формулы, которые отражают химическое строение молекул, го есть последовательное соединение их атомов, и подтвердил, что каждое вещество имеет только одну структурную формулу. Например, вещества с молекулярной формулой С5Н19 можно изобразить следующими структурными формулами, которые отражают строение трёх разных соединений, отличающихся друг от друга физическими и химическими свойствами:
Исходя из этого примера можно сделать следующий вывод.
|
|
|



 Повторите из курса 9 класса основные положения теории химического строения. Какое значение они имели для развития химии?
Повторите из курса 9 класса основные положения теории химического строения. Какое значение они имели для развития химии?
 Большинство химиков середины XIX в. вообще отрицали возможность познать структуру органических веществ. Теории, которая могла бы объяснить структуру молекул, ещё не было. Но база для этого была уже создана. Так, Э. Франкланд ввёл понятие «валентность». Ф.-А. Кекуле и А. Кольбе определили четырёхвалентность углерода и одновременно с А. Купером установили способность углерода образовывать углеродные цепи. Они предложили связи между атомами углерода обозначать чёрточкой (С—С). Но эти учёные отрицали возможность устанавливать истинное строение органических соединений по их химическим превращениям.
Большинство химиков середины XIX в. вообще отрицали возможность познать структуру органических веществ. Теории, которая могла бы объяснить структуру молекул, ещё не было. Но база для этого была уже создана. Так, Э. Франкланд ввёл понятие «валентность». Ф.-А. Кекуле и А. Кольбе определили четырёхвалентность углерода и одновременно с А. Купером установили способность углерода образовывать углеродные цепи. Они предложили связи между атомами углерода обозначать чёрточкой (С—С). Но эти учёные отрицали возможность устанавливать истинное строение органических соединений по их химическим превращениям.

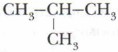 (изобутан) с последующим синтезом предсказанного изобутана.
(изобутан) с последующим синтезом предсказанного изобутана.