|
|
|
|
|
Глава 7. Альдегиды, кетоны, карбоновые кислоты и сложные эфиры Химические свойства и получение альдегидовПолучение альдегидовВам уже известно, что альдегиды находят широкое применение в жизни человека (см. § 22).
Наибольшее применение имеют формальдегид и ацетальдегид. Они же являются сырьём для получения материалов, необходимых современному человек)', поэтом)' важно знать, как их получают. Задание. Предложите возможные способы получения формальдегида и ацетальдегида и дайте им обоснование. Общим способом получения всех альдегидов является окисление спиртов. Уравнение реакции в общем виде:
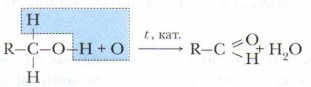
Задание. Вспомните лабораторный опыт окисления этилового спирта с помощью медной проволоки. Запишите уравнение этой реакции. Рассмотрим её схему:
В промышленных условиях метапаль, или формальдегид, получают, пропуская через реактор смесь паров метанола с воздухом над поверхностью раскалённой медной или серебряной сетки (катализатора).
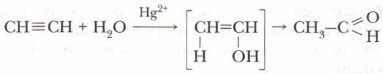
Реакция идёт в несколько стадий. Сначала происходит гидратация ацетилена по месту одной π-связи в ацетилене в присутствии солей ртути. В результате образуется непредельный виниловый спирт.
Непредельный виниловый спирт (промежуточный продукт реакции) неустойчив. Поэтому он легко переходит в уксусный альдегид.
Однако получение ацетальдегида этим способом имеет существенный недостаток из-за использования катализаторами ядовитых соединений ртути, вредных для здоровья работников, а также из-за использования дорогостоящего карбида с целью получения ацетилена.
В настоящее время разработан и внедрён более эффективный способ получения ацетальдегида каталитическим окислением этилена. Окисление этилена осуществляется кислородом в присутствии катализаторов — хлоридов палладия и меди (PdCl2 + CuCl2). Этот процесс можно представить схемой:
Данный способ получения уксусного альдегида менее вреден для здоровья, а сырьё (этилен) более доступно и дешево, чем ацетилен. Общие химические свойства альдегидов
Основные понятия Основные типы реакций альдегидов: окисления, присоединения, поликонденсации • Фенолоформальдегидная пластмасса • Качественные реакции на альдегиды • Формалин • Окисление спиртов • Способы получения ацетальдегида Вопросы и задания
Выводы 1. Альдегиды и кетоны — кислородсодержащие соединения, имеющие функциональную карбонильную группу 2. Альдегиды — это производные углеводородов, в молекулах которых карбонильная группа связана как с углеводородным радикалом, так и с атомом водорода, их функциональной группой является альдегидная группа 3. Представителями альдегидов являются формальдегид (метаналь) и уксусный альдегид (этаналь), представителем кетонов — ацетон (иропанон). 4. Свойства альдегидов обусловлены их строением. Физические свойства зависят от углеводородного радикала и изомерии. Важнейшие химические свойства альдегидов обусловлены функциональной группой. Для альдегидов характерны реакции: окисления, присоединения, замещения, а также полимеризации и поликонденсации. 5. Качественными реакциями на альдегиды являются: реакция «серебряного зеркала», реакция с Сu(ОН)2 и реакция с фуксинсернистой кислотой. 6. Альдегиды широко применяются как растворители, как сырьё для производства пластмасс, лаков и продукции фармацевтической промышленности. Получают альдегиды окислением спиртов из непредельных углеводородов, а поликонденсацией формальдегида получают фенолоформальдегидные пластмассы.
|
|
|



 Как получают фенолоформальдегидные смолы и какое они имеют значение?
Как получают фенолоформальдегидные смолы и какое они имеют значение?
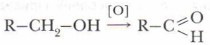
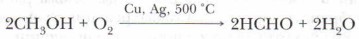
 Долгое время ацетальдегид получали в промышленности гидратацией ацетилена (реакцией Кучерова). Эта реакция синтеза была открыта в 1881 г. русским учёным М.Г. Кучеровым.
Долгое время ацетальдегид получали в промышленности гидратацией ацетилена (реакцией Кучерова). Эта реакция синтеза была открыта в 1881 г. русским учёным М.Г. Кучеровым.
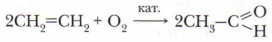
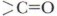 двойной связи обусловливает реакции присоединения, реакции полимеризации и поликонденсации, имеющие огромное значение для получения пластмасс.
двойной связи обусловливает реакции присоединения, реакции полимеризации и поликонденсации, имеющие огромное значение для получения пластмасс.
 1. Почему альдегидная группа определяет основные химические свойства альдегидов? Дайте обоснованный ответ.
1. Почему альдегидная группа определяет основные химические свойства альдегидов? Дайте обоснованный ответ.
 6. В чём заключается общий способ получения альдегидов? Составьте схему этого процесса и дайте к ней пояснения.
6. В чём заключается общий способ получения альдегидов? Составьте схему этого процесса и дайте к ней пояснения.
 8. Как можно различить растворы глицерина и формальдегида с помощью одного реактива? Представьте проект решения этой экспериментальной задачи.
8. Как можно различить растворы глицерина и формальдегида с помощью одного реактива? Представьте проект решения этой экспериментальной задачи.

 Названия альдегидов образуются прибавлением суффикса -аль.
Названия альдегидов образуются прибавлением суффикса -аль.