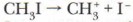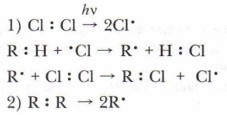|
|
|
|
|
Глава 4. Теоретические основы, механизмы и закономерности протекания реакций органических соединений § 6. Особенности и классификация органических реакций
Реакции с участием органических соединений подчиняются тем же общим законам, что и реакции неорганических веществ, их протекание также идёт по гем же закономерностям. Вместе с тем органические реакции имеют специфические особенности. 1. Большинство изученных вами реакций неорганических веществ осуществляется преимущественно в водных растворах с участием ионов и поэтому такие реакции протекают очень быстро. Органические реакции протекают значительно медленнее, чем неорганические, часто требуют жёстких условий для осуществления (повышенные температуры, давление, катализаторы). 2. Органические реакции, в отличие от неорганических, часто протекают в несколько стадий, т. е. получение их продукта идёт не через одну, а через несколько реакций, поэтому они редко дают высокий выход продукта. 3. При записи органических реакций не используют знак равенства, отражающий стехиометрические соотношения между реагентами и продуктами реакций, а приводят схемы реакций, где вместо знака равенства ставят стрелку, указывающую направление реакции, над ней записывают условия протекания реакции (температура, давление, катализатор и др.). 4. В большинстве биохимических реакций, т. е. органических реакций, протекающих в живых организмах, изменению подвергается не вся молекула органического соединения, а только её часть — реакционные центры молекулы. Важнейшими взаимосвязанными между собой характеристиками химической реакции являются: реакционная способность реагентов, скорость и механизм реакции, её энергетика. Их важно учитывать и при описании конкретных органических реакций. Три характеристики реакций вам уже известны, поэтому кратко охарактеризуем ещё одну — механизм реакции. Механизм реакцииМеханизм реакции — это описание её пути, т. е. последовательность элементарных стадий, через которые проходят реагенты, превращаясь в продукты реакции. Большинство реакций органических веществ и практически все биохимические реакции — сложные. Механизм реакции служит основой одной из классификаций реакций в органической химии. Нуклеофил — это частица, которая атакует атом углерода, предоставляя ему электронную пару (т. е. является донором электронов). Как правило, такие частицы обладают основными свойствами. К нуклеофилам относятся ОН-, Cl-, S2-, Электрофил — это частица, которая атакует атом углерода органического соединения, отнимая у него электронную пару (является акцептором электронов), размещаемую на свободную орбиталь электрофила. Примерами частиц-электрофилов могут служить: Н3О+, Н+, HCI, HNO3, Итак, нуклеофилы — доноры электронов, электрофилы — их акцепторы. Если мы обратимся к ряду напряжений, то обнаружим, что ряд катионов (восстановители) проявляют нуклеофильные свойства, а анионы (окислители) — электрофильные.
В зависимости от способа разрыва ковалентных связей в атакующем реагенте определяется механизм реакции.
В органической химии выделяют два основных механизма реакции: радикальный (гомолитический) и ионный (гетеролитический).
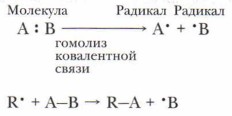
Вы уже знаете, что при химических реакциях происходит разрыв одних и образование других химических связей. Эти два противоположных процесса осуществляются в единстве. Разрыв ковалентной связи в исходных соединениях в органических реакциях может осуществляться двумя разными способами. 1. Радикальный (гомолитический) разрыв ковалентной связи (гомолиз) (от греч. homos — «равный», «одинаковый» и lysis — «растворение», «распад»). В этом случае происходит симметричный разрыв ковалентной связи (общей электронной пары) и у каждой образующейся частицы остаётся по одному неспаренному электрону.
Образовавшиеся частицы называются радикалами. Примерами свободных радикалов являются частицы: •СН3, Сl•, •СН3СН2 и др. Радикальному (гомолитическому) разрыву, или гомолизу, обычно подвергаются неполярные или малополярные ковалентные связи (С—С, С—Н, Cl—Cl, N—N, Вr—Вr и др.). Гомолиз осуществляется при определённых условиях (высокая температура, действие света, радиоактивное облучение), а также при проведении реакций в газовой фазе, например: СН3— СН2— СНЧ → СН3—СН2• + •СН3.
2. Ионный (гетеролитический) разрыв ковалентной связи (гетеролиз) (от греч. heteros — «другой», «иной» и lysis — «распад»).
Частица В, захватывая чужой электрон, превращается в отрицательно заряженный ион — анион В- (нуклеофил). Происходит гетеролиз ковалентной связи. К гетеролитическому разрыву склонны полярные и легко поляризуемые связи. Например:
Гетеролизу способствуют полярные растворители.
Классификация реакций органических соединенийЧтобы ориентироваться в многообразии реакций органических соединений и облегчить процесс их усвоения, необходима их классификация. Для осуществления этой логической операции надо выбрать наиболее общие классификационные признаки. Безусловно, реакции органических веществ, как и неорганических, могут быть: экзотермическими и эндотермическими; гомогенными и гетерогенными, каталитическими и некаталитическими, обратимыми и необратимыми и т. д. Их также можно классифицировать по составу исходных веществ и продуктов реакции. Все они имеют одинаковые общие признаки и подчиняются общим законам протекания химических реакций. Вместе с тем эти реакции имеют свои особенности, которые обусловлены особенностями строения органических соединений. Большинство реакций органических соединений включает несколько последовательных процессов, или стадий. Они характеризуются определённым направлением, а образование продуктов реакции идёт через определённые стадии. В связи с этим их принято классифицировать по механизмам протекания, по направлению и конечным продуктам реакции. Классификация реакций органических веществ по механизму реакции (по характеру разрыва ковалентной связи реагента)1. Гомолитические (радикальные) реакции идут с образованием радикалов — частиц с неспаренным электроном. Их течение сопровождается гомолитическим разрывом ковалентной связи. Эти реакции протекают в газообразной фазе или в неполярных растворителях, требуют высокой температуры или воздействия светом. Запишем схему процесса:
Примером гомолитической реакции является хлорирование алканов по свободнорадикальному цепному механизму. Эта реакция идёт через определённую последовательность элементарных процессов, или стадий, она является цепной, г. к. первая стадия инициирует развитие последующих стадий:
Таким образом, механизм цепной реакции, рассмотренный выше, например хлорирования метана, принимает следующий вид:
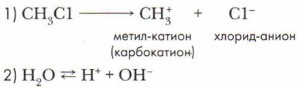
2. Гетеролитические (электрофильные-нуклеофильные, или ионные) реакции происходят без разрыва электронных пар, образующих химические связи: оба электрона переходят на орбиталь одного из атомов продукта реакции с образованием катиона и аниона. Такие реакции сопровождаются гетеролитическим расщеплением ковалентной полярной связи и образованием ионов. К гетеролитическому разрыву склонны сильно полярные и легко поляризуемые связи. Гетеролитический распад ковалентной полярной связи приводит к образованию нуклеофилов (анионов) и электрофилов (катионов):
Образовавшиеся органические ионы вступают в дальнейшие превращения, например:
В зависимости от природы атакующего реагента реакции могут быть нуклеофильными или электрофильными.
Нуклеофильными называются реакции органических соединений с нуклеофильными реагентами (нуклеофилами), т. е. анионами или молекулами, которые предоставляют свою пару электронов на образование новой связи.
Примером такой реакции может служить взаимодействие бромметана с гидроксидом натрия:
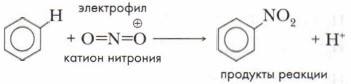
Электрофильными называются реакции органических соединений с электрофильными реагентами (электрофилами), т. е. катионами или молекулами, которые имеют свободную орбиталь, готовую принять электроны для образования новой связи. Примером такой реакции может служить реакция нитрования бензола:
Эти же реакции могут быть включены и в другую классификацию по продуктам реакции.
|
|
|



 Что происходит с веществами в процессе химической реакции? На примере конкретной реакции дайте пояснение.
Что происходит с веществами в процессе химической реакции? На примере конкретной реакции дайте пояснение.
 Химическая реакция между двумя реагентами может рассматриваться как атака одной частицы (молекулы, атома, радикала, иона и т. д.) на другую. Среди атакующих частиц различают нуклеофил и электрофил.
Химическая реакция между двумя реагентами может рассматриваться как атака одной частицы (молекулы, атома, радикала, иона и т. д.) на другую. Среди атакующих частиц различают нуклеофил и электрофил.

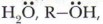 СН3O- и др.
СН3O- и др.
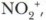 АlСl3 и др.
АlСl3 и др.
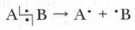
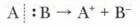
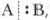 приобретает положительный заряд и превращается в катион А+ (электрофил).
приобретает положительный заряд и превращается в катион А+ (электрофил).