|
|
|
|
|
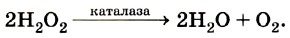
Практическая работа № 9 Практическая работа № 9. Действие ферментов на различные веществаДействие амилазы слюны на крахмалТщательно прополощите рот водой. Наберите 2— 4 мл слюны в маленький мерный цилиндр. Добавьте в цилиндр воды до объёма в 10 мл. Полученный раствор содержит фермент амилазу, который вы и будете изучать. Смешайте 5 мл раствора крахмала и 1 мл раствора фермента в маленькой мензурке или пробирке. Через 30 с после перемешивания возьмите каплю полученного раствора и проверьте её на содержание крахмала, перемешав её с каплей раствора иода на предметном стекле. Спустя ещё 30 с проверьте следующую каплю смеси на содержание крахмала. Если крахмал ещё присутствует, то повторяйте тест каждые 30 с до тех пор, пока больше не обнаружите крахмала в смеси. Запишите общее время, необходимое для того, чтобы исчез весь крахмал. Две новые порции смеси растворов фермента и крахмала (2,5 мл раствора крахмала и 0,5 мл раствора фермента) в двух пробирках поместите в стаканчики с водой: в одном вода охлаждена с помощью льда или снега до температуры 10 °С, а другой — с тёплой водой при 35—40 °С (приблизительно). Каждые 30 с отбирайте по 1 капле смеси растворов крахмала и фермента и смешивайте с каплей раствора иода на предметном стекле. Повторяйте это, пока не обнаружите, что в растворе исчез крахмал. Запишите затраченное время, сделайте вывод о влиянии температуры на работу фермента. Действие дегидрогеназы на метиленовый синий (стиральная синька)Аптечный формалин разбавьте водой до получения 0,5% -го раствора формальдегида (с учётом его первоначальной концентрации). В две пробирки налейте по 5 мл некипячёного молока (лучше свежего), добавьте с помощью пипетки по 15 капель 0,5%-го раствора формальдегида и по 5 капель (с помощью другой пипетки) раствора метиленового синего (можно и просто разбавленных синих чернил). Краситель постепенно бледнеет, обесцвечивается. Это происходит потому, что к его молекуле присоединяется водород, «отобранный» у формальдегида при участии фермента дегидрогеназы (объясните этимологию названия фермента), который содержится в коровьем молоке. Налейте в обе пробирки немного подсолнечного масла, чтобы изолировать реакционную смесь от воздуха и таким образом предотвратить окисление обесцвеченного красителя кислородом воздуха. Первую пробирку поставьте в пустой стаканчик, а вторую поместите в стаканчик с тёплой водой (35— 40 °С). Отметьте, что особенно быстро краситель будет обесцвечиваться во второй пробирке, температура которой близка к температуре тела млекопитающих. Это «работает» дегидрогеназа: она переносит атомы водорода от формальдегида к метиленовому синему. Продуйте с помощью стеклянной трубки и резиновой груши через реакционную смесь воздух — краситель снова восстановит свой цвет. Действие каталазы на пероксид водородаКаталаза — это фермент, катализирующий разложение пероксида водорода:
Пероксид водорода образуется в некоторых растительных и животных клетках в качестве побочного продукта обмена веществ. Соединение это токсично для клеток, и каталаза обеспечивает эффективное его удаление. Это один из наиболее быстро работающих ферментов: при О °С одна молекула каталазы разлагает в 1 с до 50 000 молекул пероксида водорода. Налейте в пробирки по 2 мл раствора перекиси водорода (имеющегося в каждой аптечке). В первую пробирку опустите с помощью пинцета кусочек сырого мяса. Что наблюдаете? Поднесите к отверстию пробирки тлеющую лучинку. Что наблюдаете? Во вторую пробирку опустите кусочек сырого картофеля и поднесите к отверстию тлеющую лучинку. Что наблюдаете? Возьмите кусочек сырого картофеля, приблизительно такой же, какой использовали в предыдущем опыте, положите его в ступку с небольшим количеством мелкого чистого песка. Измельчите пестиком песок с картофелем и перенесите полученный материал в третью пробирку. Можно измельчить картофель и на крупной тёрке. Обратите внимание на большую активность размельчённой ткани картофеля по сравнению с его целым кусочком. Почему? В четвёртую и пятую пробирки опустите по кусочку варёного мяса и варёного картофеля. Что наблюдаете? Почему?
|
|
|